Рча улв что это
РЧА (Радиочастотная катетерная абляция)
Метод радиочастотной катетерной абляции был разработан и внедрен в медицинскую практику в 80-х годах ХХ века и с тех пор стал одним из основных способов лечения аритмий во всем мире.
Радиочастотная катетерная абляция является эффективной заменой многим ранее применявшимся хирургическим операциям на открытом сердце, а также признана современной медициной в качестве прекрасной альтернативы приему фармакологических препаратов. В клинике ЦЭЛТ это вмешательство выполняют высококвалифицированные специалисты, используя самое современное оборудование и ориентируясь на европейские медицинские стандарты.
Как проводится РЧА?
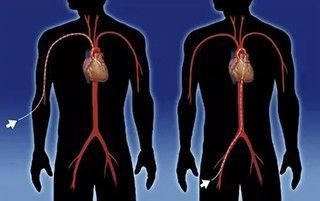
Вся операция обычно выполняется под местной анестезией. Врачи прокалывают пациенту бедренную вену или артерию, что зависит от тех отделов сердца, на которых планируется осуществить вмешательство, и подключичную вену. Через имеющиеся проколы при помощи специальных трубочек в полость сердца пациента вводятся электроды. Данная манипуляция выполняется под тщательным рентгеноскопическим контролем.
На первом этапе операции проводится подробное электрофизиологическое исследование сердца (ЭФИ), результатом которого должно стать обнаружение зон, провоцирующих возникновение аритмии. Информация о деятельности сердца во время ЭФИ поступает на компьютерные мониторы, формируя внутрисердечную кардиограмму.
Во время исследования на сердечной мышце проводятся специальные тесты, призванные спровоцировать возникновение аритмий. Пациент при этом может испытывать дискомфортные ощущения в грудной клетке, некоторую болезненность и сердцебиения. Но бояться перебоев в работе сердца, внезапного ускорения или замедления его ритма в ходе выполнения ЭФИ не стоит. При помощи электрических импульсов, которые подаются электродами непосредственно в сердце, кардиохирург полностью контролирует сердечную деятельность, провоцируя аритмические приступы и прекращая их в процессе поиска аритмогенных участков.
Радиочастотная катетерная абляция (РЧА) сердца.
Радиочастотная катетерная абляция (РЧА) сердца.
РЧА сердца – хирургическое катетерное вмешательство, с использованием специальных катетеров, пункционно введенных в полость сердца через сосуды, и радиочастотной энергии, направленное на устранение нарушений сердечного ритма (аритмии).
Радиочастотная абляция — один из самых современных методов лечения некоторых видов нарушений ритма сердца. Этот вид лечения относится к малоинвазивным вмешательствам, так как для его проведения не требуется никаких разрезов и доступов к сердцу, но иногда РЧА выполняется при операциях на открытом сердце. Радиочастотная абляция проводится с помощью тонкого гибкого катетера-проводника, который вводится через кровеносный сосуд и подводится к источнику неправильного ритма в сердце, вызывающего аритмию. Далее по этому проводнику подается радиочастотный импульс, который разрушает участок ткани, отвечающий за неправильный ритм. Впервые высокочастотную энергию для устранения дополнительных АВ-путей проведения, применяемую и по сей день, произвели в 1986 году М.Borggrefe и соавт. С этого времени и началось бурное развитие интервенционной аритмологии в лечении аритмий сердца.
Подобная деструкция патологического очага может осуществляться также путем прочих физических воздействий, в соответствии с чем выделяют и другие виды абляции:
Показаниями к проведению РЧ-абляции являются нарушения сердечного ритма, которые уже невозможно скорректировать медикаментозно:
Наряду с показаниями к РЧА, абляция имеет и перечень противопоказаний:
Радиочастотная (РЧ) энергия имеет широкий диапазон и зависит от сопротивления и диэлектрических свойств тканей. Радиочастотный ток – это ток с меняющейся полярностью при частоте от 30 кГц до 300 МГц. Все генераторы РЧ тока, используемые для аблации, работают в диапазоне 300 кГц — 1 МГц. Для аблации структур сердца применяют немодулированный ток, поскольку именно он приводит к образованию коагуляционного некроза.
Существует два варианта подачи электрической энергии: монополярный и биполярный. При монополярной аблации переменный ток проходит между дистальным концом «активного» электрода через ткани к «пассивному» электроду на поверхности грудной стенки. Обычно «пассивным» или референтным электродом служит пластина. Эксперименты показали, что позиция пластины незначительно влияет на размер воздействия, в то время как увеличение ее площади ведет к отклонению импеданса и приводит к увеличению энергии и перегреву электрода. В случае биполярной коагуляции ток проходит между двумя активными электродами в полостях сердца.
Прогрессивное воздействие достигается благодаря созданным устройствам контроля температуры высокочастотной энергии (Haverkampf et al. 1991). Контроль температуры означает, что температура на конце катетера не только изменяется в течение процесса коагуляции, но и поддерживается на определенном уровне благодаря механизму обратной связи для подаваемой мощности. Такое устройство позволяет создавать ограниченное поражение с предсказуемой степенью in vitro и обеспечивает хороший контакт между электродом, вызывающим аблацию, и миокардом. Мониторинг температуры становится практически сложным при увеличении размера электрода или его геометрии. Так, например, для линейной аблации ФП и ТП используются удлиненные электроды, имеющие одну термопару, таким образом невозможно предсказать какой стороной происходит контакт поверхности электрода с эндокардом и температура краевой повехности может оказаться намного выше, чем тела электрода, где расположен термодатчик. Таким образом, температура в серединной точке остается недооцененной.
В некоторых экспериментальных исследованиях продемонстрирован трехмерный окончательный элементарный анализ влияния геометрии электрода, угла наклона контакта электрод-ткань и циркуляции окружающей крови на размер аблационного повреждения.
Длительность радиочастотной аблации так же является важным критерием, влияющим на трансмуральность воздействия. Наибольшее увеличение размера повреждения происходит в течение первых 30 секунд аблации, а затем наступает плато.
Некоторое усовершенствование аблации было достигнуто в результате использования электрода с охлаждением наконечника инфузией физиологического раствора. Такая конструкция позволяет использовать высокие цифры энергии воздействия, увеличивая размер повреждения, но избегая при этом высоких цифр импеданса. Эта концепция была подтверждена в экспериментах in vivo и in vitro. Охлаждение в течение аблации приводит к повышению температуры глубже поверхности эндокарда. Максимальная температура регистрируется на глубине 1 мм и более от поверхности эндокарда, таким образом даже выше, чем в области контакта электрода с поверхностью эндокарда. Катетеры для холодовой аблации могут быть закрытого типа, когда охлаждающий раствор циркулирует внутри системы и открытого типа, имеющие маленькие дырочки через которые происходит орошение электрода и жидкость вытекает наружу.
Таким образом, радиочастотная аблация является безопасной и эффективной методикой. В ходе проведения экспериментальных исследований не отмечено возникновения таких серьезных осложнений, как аритмии, расстройства гемодинамики, ишемия, тромбоз или эмболия. Наибольшую опасность представляет собой перегревание и последующее повреждение аблационного катетера и выпаривание ткани. С целью ограничения риска этих осложнений многие исследователи считают необходимым проводить измерение биофизических параметров (сила тока, напряжение, температура) на конце катетера.
Возможные осложнения РЧА сердца делятся на 4 группы:
4.Осложнения, обусловленные радиочастотным воздействием (АВ-блокада)
5. Случайное нарушение целостности тканей сердечной мышцы в момент абляции.
6. Сбои в работе электрической системы сердца, усугубляющие нарушение сердечного ритма и требующие трансплантации кардиостимулятора.
7. Стеноз легочных вен, т. е. сужение их просвета.
Осложнения после РЧА сердца крайне редки: вероятность негативных последствий абляции не превышает 1%. Потому РЧА причисляется к категории операций с малой степенью риска. Однако для профилактики осложнений существует ряд специальных мер, принимаемых на каждом из этапов обнаружения и лечения тахикардии.
Риск подобных осложнений повышается в тех случаях, когда пациент является диабетиком, если у него нарушена свертываемость крови, а также если он преодолел 75-летний возрастной порог.
Данная операция относится к классу малоинвазивных вмешательств. Преимущества же такого хирургического вмешательства очевидны: минимальная травматичность, как правило, отсутствие необходимости в назначении общей анестезии, небольшая продолжительность операции, короткий послеоперационной койко-день
Как подготовиться к РЧА.
Подготовка к данной операции заключается в проведении электрофизиологического исследования (ЭФИ) сердца. Необходимость РЧА у конкретного пациента констатируется его лечащим врачом на основании истории заболевания и данных таких диагностических методов, как:
После регистрации с помощью ЭКГ приступа тахикардии пациент госпитализируется в стационар для прохождения полного курса обследования и сдачи перечня необходимых анализов, на основе которых ему может быть назначена радиочастотная абляция сердца:
Общие принципы подготовки к операции включают в себя:
• Последний прием пищи вечером накануне операции (12 часов голода).
• В месте установки катетера (паховая и подключичная область) должны быть выбриты волосы
• В ночь перед исследование проводиться очищение кишечника.
• Спросите своего врача, следует ли вам принимать обычные лекарства утром.
• Все антиаритмические препараты отменяются за 2–3 дня до исследования (пять периодов полувыведения), для кордарона это 28 дней.
• Если у вас сахарный диабет, спросите своего врача, следует ли Вам принимать инсулин или другие сахароснижающие пероральные препараты перед исследованием.
Методика проведения РЧА сердца.
РЧА сердца проводится в плановом порядке в специально оборудованной операционной, оснащенной:
• рентгенотелевизионной системой для рентгеноскопии и/или рентгенографии;
• оборудованием для слежения за жизненно важными функциями организма и проведения реанимационных мероприятий (дефибриллятор, дыхательный аппарат, мониторы);
• специализированным ЭФИ-оборудованием для записи поверхностных электрокардиограмм и внутрисердечных электрограмм и снабженным
• специализированным электрокардиостимулятором и набором инструментов для проведения катетеризации сердца и электродов-катетеров для проведения ЭФИ и РЧА;
• защитным оборудованием для пациента и персонала (костюмы, фартуки, очки, передвижные стенки и т. д.).
Пациент для проведения операции РЧА поступает в операционную натощак, в слегка седатированном состоянии. Области предполагаемых пункций сосудов тщательно обрабатываются и накрываются стерильным бельем. Проведение катетеров всегда производится с использованием чрескожной техники. Для пункции используются обычно бедренные вены справа и/или слева, подключичная вена слева и/или справа и яремная вена справа, а также вены предплечья. Для артериального доступа обычно используется правая бедренная артерия, однако возможна пункция бедренной артерии слева и лучевых артерий.
Местная анестезия места пункции, после этого производится пункция вены с помощью иглы, которая вводится в сосуд, и проводится необходимой длины проводник, после чего игла вытаскивается. Далее по проводнику вводится интродьюсер, а затем электрод-катетер в соответствующую камеру сердца. Разместив катетеры в различных камерах сердца, их подключают к соединительной коробке, которая переносит электрические сигналы от электродов в сердце к записывающему оборудованию и позволяет стимулирующему импульсу от ЭКС достигать поверхности различных камер сердца. Выполняется ЭФИ сердца. Электрические сигналы, полученные от эндокардиальной поверхности сердца, фильтруются, усиливаются и выводятся на мониторе компьютера. Программируемый ЭКС должен обладать способностью для постоянной и программируемой стимуляции, подачи множества экстрастимулов (до 7), регулировки амплитуды и длительности импульса, а также возможностью воспринимать внешние и внутрисердечные сигналы.
При проведении ЭФИ пациент может ощущать дискомфорт в грудной клетке, сердцебиения, небольшую болезненность. Ощущения, возникающие при проведения ЭФИ, в виде перебоев сердца, секундных остановок, ускорения или замедления ритма являются результатом работы врача, т.е с помощью электрических импульсов, подаваемых непосредственно в сердце, врач полностью контролирует сердцебиение, провоцируя приступ сердцебиения или прекращая его во время поиска аритмогенных участков. При обнаружении аритмогенных зон (дополнительных предсердно-желудочковых соединений, эктопической активности и т. п.) на нее воздействуют радиочастотной энергией с помощью «лечебного» электрода. После чего в обязательном порядке (примерно через 20 минут) проводят еще раз ЭФИ для оценки эффективности воздействия. Если электрофизиологические показатели удовлетворяют врача, то операцию заканчивают. Удаляют катетеры. На места пункций накладывают гемостатические (давящие) повязки.
Вас переводят в отделение и назначают постельный режим в положении на спине на несколько часов (в некоторых случаях до суток) с целью предупреждение кровотечения из места пункции. Наблюдение в стационаре от одного до 3 дней.
Хирургическое лечение фибрилляции предсердий
Фибрилляцией предсердий (ФП) в медицинской терминологии называется нарушение ритма сердца (мерцательная аритмия). Оно может быть спровоцировано повышенным количеством электрических контуров в предсердиях, которые приводят к беспорядочным сокращениям желудочков сердца и к недостаточности эффективного сокращения предсердий. Это, в свою очередь, становится причиной образования сгустков крови в предсердиях, что может в итоге привести к закупорке сосудов головного мозга и смерти пациента.
Среди основных методов лечения при мерцательной аритмии на сегодняшний день – медикаментозная терапия, катетеризация, а также хирургическая лабиринтная методика (Maze) – довольно сложная и потому не очень популярная среди кардиохирургов.
«Новым словом» в лечении мерцательной аритмии стала радиочастотная абляция сердца (РЧА) устьев легочных вен – малоинвазивная операция путем небольших проколов, осуществляемая с применением последних компьютерных технологий и в условиях постоянного рентгеновского контроля.
После абляции: хаотичные импульсы, провоцирующие аритмию, не могут попадать в полость предсердия
Реабилитация после РЧА
В целом реабилитация после РЧА длится несколько месяцев, в течение которых пациенту может быть назначен прием антиаритмических препаратов (к примеру, «Пропафенон», «Пропанорм» и др.), в том числе и тех, которые больной принимал до абляции. Постельный режим с контролем сердечного ритма и артериального давления показан больному лишь в самые первые сутки после операции, в течение которых происходит быстрое восстановление и стабилизация нормального общего самочувствия пациента. Необходимость же повторной РЧА, как показывает практика, у прооперированных пациентов возникает реже, если пациент пересмотрит свой привычный образ жизни:
Результаты абляции
Абляция сердца может быть успешной, но некоторым больным приходится повторять процедуру. Возможно, придется принимать лекарственные препараты, даже после проведения абляции.
Рча улв что это
РЧА в кардиологии. Показания и противопоказания.
В настоящее время радикально решить проблему ускоренного проведения импульсов по сердечной мышце, лежащую в основе тахикардии, позволяет операция радиочастотной абляции (РЧА), или методика “прижигания сердца”. С помощью данной методики ликвидируется небольшой участок ткани, осуществляющий патологически частое возбуждение сердечной мышцы. Это осуществляется путем воздействия на ткань радиочастотных сигналов, оказывающих повреждающее действие. В результате дополнительный путь проведения импульсов прерывается, в то же время нормальные пути проведения импульсов не повреждаются, и сердце сокращается в своем обычном ритме, с частотой 60-90 ударов в минуту.
Показания для операции
Основными показаниями для проведения радиочастотной катетерной абляции являются нарушения ритма по типу тахикардии или тахиаритмии. К ним относятся:
Мерцательная аритмия – нарушение ритма, при котором мышечные волокна предсердий сокращаются по отдельности, изолированно друг от друга, а не синхронно, как при нормальном ритме. При этом создается механизм циркуляции импульса, и возникает патологический очаг возбуждения в предсердиях. Это возбуждение распространяется на желудочки, которые начинают также часто сокращаться, что вызывает ухудшение общего состояния пациента. Частота сердечных сокращений при этом достигает 100 – 150 ударов в минуту, иногда более.
Желудочковая тахикардия – частое сокращение желудочков, опасное тем, что быстро, еще до оказания помощи, может развиться фибрилляция желудочков и остановка сердца (асистолия).
ВПВ – синдром – заболевание, обусловленное врожденными нарушениями в проводящей системе сердца, в результате чего сердечная мышца предрасположена к опасным пароксизмальным тахикардиям.
Хроническая сердечная недостаточность и кардиомегалия (расширение полостей сердца), вследствие чего возникают нарушения ритма сердца.
Противопоказания
Несмотря на доступность и малую травматичность метода, он имеет свои противопоказания. Так, метод РЧА не может быть применен, если у пациента наблюдаются следующие заболевания:
Острый инфаркт миокарда,
Лихорадка и острые инфекционные заболевания,
Обострение хронических болезней (бронхиальная астма, декомпенсация сахарного диабета, обострение язвенной болезни желудка и др),
Тяжелая почечная и печеночная недостаточность.
Подготовка к процедуре
Госпитализация в стационар, где будет проводиться абляция, осуществляется в плановом порядке. Для этого пациент должен быть максимально обследован в поликлинике по месту жительства лечащим аритмологом, а также ему необходимо получить консультацию кардиохирурга.
Перечень обследования перед операцией включает в себя:
Общие анализы крови и мочи,
Анализ свертывающей системы крови – МНО, протромбиновое время, протромбиновый индекс, АЧТВ, время свертывания крови (ВСК),
УЗИ сердца (эхокардиоскопия),
ЭКГ, а при необходимости мониторирование ЭКГ по Холтеру (оценка сердечного ритма по ЭКГ за сутки),
ЧПЭФИ – чрезпищеводное электрофизиологическое исследование – может понадобиться в том случае, если врачу необходимо точнее установить локализацию источника патологического возбуждения, а также если нарушения ритма по ЭКГ не регистрируются, хотя у пациента сохраняются жалобы на приступообразное учащенное сердцебиение,
Пациентам с ишемией миокарда может быть показано проведение коронароангиографии (КАГ) перед операцией,
Исключение очагов хронической инфекции – консультация стоматолога и ЛОР-врача, а также уролога для мужчин и гинеколога для женщин – как и перед любой операцией,
Исследование крови на ВИЧ, вирусные гепатиты и сифилис.
После того, как пациент запланирован на операцию, он должен госпитализироваться в стационар за два-три дня до назначенной даты. За сутки до операции следует отказаться от приема антиаритмических или иных препаратов, могущих оказывать влияние на сердечный ритм, но только по согласованию с лечащим врачом.
Возможные осложнения
Операция абляции является малотравматичной, поэтому осложнения могут появиться в крайне редких случаях (менее 1%). Тем не менее, регистрируются следующие неблагоприятные состояния после операции:
Инфекционно-воспалительные – нагноения кожи в месте пункции, инфекционный эндокардит (воспаление внутренней полости сердца),
Тромбоэмболические осложнения – формирование тромбов вследствие травматизации сосудистой стенки и распространение их по сосудам внутренних органов,
Нарушения сердечного ритма,
Прободение артерий и стенки сердца катетером и зондом.
Образ жизни и прогноз после операции
Образ жизни после операции должен соответствовать следующим принципам:
Рациональное питание. В связи с тем, что основной причиной нарушений ритма сердца является ишемическая болезнь сердца, следует стремиться к профилактическим мерам, снижающим уровень”вредного” холестерина в плазме крови и предупреждающим его отложение на стенках сосудов, питающих сердечную мышцу. Самым главным из подобных мероприятий является снижение потребления животных жиров, продуктов фаст-фуд, жареной и соленой пищи. Приветствуется употребление зерновых, бобовых культур, растительных масел, нежирных сортов мяса и птицы, кисломолочных продуктов.
Адекватные физические нагрузки. Заниматься легкой гимнастикой, ходьбой и легким бегом полезно для здоровья сердца и сосудов, но должно быть начато через несколько недель после операции и только по разрешению лечащего врача.
Отказ от вредных привычек. Учеными давно доказано, что курение и алкоголь не только повреждают стенку сосудов и сердце изнутри, но и могут оказывать прямой аритмогенный эффект, то есть провоцировать пароксизмальные тахиаритмии. Поэтому прекращение курения и отказ от крепких спиртных напитков в больших количествах является профилактикой нарушений ритма.
В заключение необходимо отметить – несмотря на то, что РЧА является хирургическим вмешательством в организм, риск осложнений сравнительно не велик, а вот польза от операции несомненна – большинство пациентов, судя по отзывам, перестают испытывать неприятные симптомы и менее подвержены риску сосудистых катастроф, связанных с пароксизмами тахиаритмий.
Главный врач
БОНДАРЬ ВАЛЕРИЙ ВАСИЛЬЕВИЧ
Главный врач ГБУЗ «Никольская районная больница» ведёт личный приём граждан каждый понедельник и четверг с 13-00 до 16-00. Вы имеете возможность также задать вопрос в электронном виде.
Рча улв что это
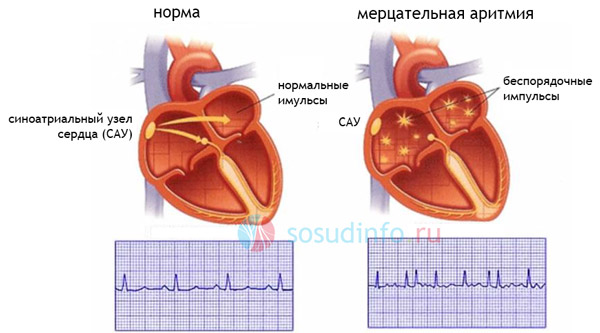
В норме регулярная работа нашего сердца поддерживается электрическими импульсами, которые генерируются группой специальных клеток. Эти клетки сформированы в компактное образование – синусовый узел, расположенный в верхней части правого предсердия [рис. 1].
При фибрилляции предсердий (мерцательной аритмии) вместо регулярного сердечного ритма в предсердиях возникают множественные электрические волны, приводящие к хаотичным сокращениям обоих предсердий с очень высокой частотой [рис. 2].
Фибрилляция предсердий (мерцательная аритмия), как правило, проявляется учащенным нерегулярным сердечным ритмом, одышкой, плохой переносимостью физических нагрузок. Нередко фибрилляции предсердий протекает бессимптомно и обнаруживается случайно при регистрации ЭКГ. Нередко у пациентов с фибрилляцией предсердий (мерцательной аритмии) обнаруживается еще один вид нарушений сердечного ритма – трепетание предсердий [ рис.3 ]. Симптомы трепетания предсердий мало отличаются от фибрилляции предсердий. Точная диагностика данных нарушений ритма и определение тактики лечения должны определяется кардиологом-аритмологом.
2. Зачем и как лечить фибрилляцию предсердий?
Лечение фибрилляции предсердий ставит своей целью:
По данным мировой медицинской статистики фибрилляция предсердий (мерцательная аритмия) – самое часто встречающаяся (1-2 % в популяции) нарушение сердечного ритма. У значительной части пациентов (до 40%) ФП носит бессимптомный характер. У этой категории больных медикаментозное антиаритмическое или немедикаментозное лечение (катетерная аблация) ФП, как правило, не проводится. Лечение этих пациентов заключается в контроле частоты сердечного ритма и назначении антикоагулянтов для профилактики тромбоэмболических осложнений. Пациентам, у которых фибрилляция предсердий сопровождается описанными выше симптомами назначают постоянную антиаритмическую терапию, направленную на профилактику рецидивов ФП. Приблизительно у одной трети среди всех больных ФП удается подобрать эффективный антиаритмический препарат или их комбинацию.
У 30% больных с симптомной, плохо переносимой фибрилляцией предсердий не удается подобрать эффективную антиаритмическую терапию, либо прием антиаритмических средств противопоказан, сопровождается развитием побочных эффектов или пациенты не хотят придерживаться тактики длительного консервативного медикаментозного лечения. Этой категории больных в соответствии с современными международными и российскими рекомендациями рекомендуется проведение катетерной аблации.
Следует подчеркнуть, что выбор вариантов лечения в каждом конкретном случае – задача кардиолога-аритмолога с учетом мнения пациента и объективных медицинских данных.
3. Катетерная и хирургическая аблация
В зависимости от формы фибрилляция предсердий (пароксизмальная, персистирующая или постоянная), наличия другой патологии со стороны сердечно-сосудистой системы и сопутствующих заболеваний применяются 3 разновидности катетерной (или хирургической) аблации:
• внутрисердечная катетерная аблация – наиболее широко используемый метод немедикаментозного лечения ФП. Катетерная аблация проводится в условиях рентгеноперационной с использованием управляемых катетеров, перемещаемых в камеры сердца через сосудистые доступы (бедренные и подключичные вены). Цель катетерной аблации радикальное устранение «источников» аритмии в левом и (при трепетании предсердий) правом предсердии. В настоящее время широкое клиническое применение нашли 2 вида катетерной аблации: радиочастотная катетерная аблация и баллонная криоаблация.
• катетерная аблация (деструкция) АВ узла – разновидность внутрисердечной катетерной аблации, которая применяется в тех случаях, когда ФП сопровождается стойко высокой частотой сердечных сокращений при невозможности медикаментозного контроля или радикального устранения ФП. Аблация АВ узла проводится только после имплантации искусственного водителя ритма (кардиостимулятора).
4. Радиочастотная или баллонная криоаблация?
Как это работает?
Видео 1. Баллонная криоаблация
Эффективность и безопасность
Общепринятым определением эффективности катетерной аблации при ФП считается отсутствие любых предсердных аритмий после аблации без применения антиаритмических средств. Контроль за эффективностью осуществляется клинически (самоконтроль пациентов) или с использованием систем длительной регистрации ЭКГ (ХМ ЭКГ или специальные имплантируемые регистраторы сердечного ритма).
Одним из основных факторов, определяющих эффективность катетерных аблаций при ФП является длительность эпизодов фибрилляции. В тех случаях когда приступы аритмии не превышают нескольких часов или дней (т.н. пароксизмальная форма) и, как правило, закачиваются самостоятельно, оперативное лечение максимально эффективно. В сравнительных исследованиях (международное исследование «Fire and Ice») рецидивов ФП в течение первого года не было у 65% больных как после радиочастотной, так и после баллонной криоаблации. При этом, есть наблюдения, что у лиц без сопутствующей кардиальной патологии эффективность баллонной криоаблации может достигать 80-90%.
У пациентов с персистирующей формой ФП, т.е. с аритмией длительностью более 7 дней, а также требующей для восстановления синусового ритма проведения медикаментозной или электрической кардиоверсии, ожидаемая эффективность катетерных аблаций – около 50-60%.
Если после катетерной аблации ФП рецидивирует с прежней частотой и длительностью, оправданным является проведение повторного вмешательства.
Осложнения при катетерной аблации ФП могут проявляться в виде повреждения сосудов в месте пункции, перфорации стенки сердца с развитием тампонады, образование тромбов в полости сердца и тромбоэмболическими осложнениями, термическим повреждением пищевода, развитием пареза диафрагмального нерва и рядом других. Применение современных высокотехнологичных методов контроля во время внутрисердечных вмешательств, достаточный опыт и квалификация врачей позволяет выполнять данные вмешательства эффективно и без значительного риска развития осложнений. Вместе с тем, необходимо четко осознавать, что решение о проведении интервенционного лечения ФП должен принимать врач с достаточным опытом лечения подобной категории больных, объективно учитывая аргументы «за и против».
5. Катетерная аблация ФП в отделе клинической электрофизиологии и рентгенхирургии нарушений ритма
Интервенционная аритмология – одно из основных направлений в научной и клинической работе отдела клинической электрофизиологии с момента его основания в 1990 г. Почти 20 лет насчитывает опыт лечения различных нарушений сердечного ритма с использованием технологии катетерных аблаций.
С 2012 года в отделе был внедрен метод катетерных аблаций при ФП. Сегодня приоритетным методом, используемым в клинической практике отдела клинической электрофизиологии при немедикаментозном лечении ФП является метод баллонной криоаблации. Этот выбор основан на том, что криоаблация при ФП не уступает по эффективности радиочастотной, являясь при этом наиболее безопасным методом интервенционного лечения ФП, что было доказано при анализе многолетнего опыта ведущих мировых центров в лечении ФП.
Специалисты отдела клинической электрофизиологии проводят полноценное предоперационное обследование пациентов, выполняют интервенционное вмешательство и обеспечивают амбулаторное наблюдение за всеми пациентами в течение не менее 1 года после катетерной криоаблации ФП. В тех случаях, когда у пациентов имеются сложные сопутствующие нарушения сердечного ритма применяется комплексное (одномоментное) интервенционное лечение, либо т.н. «гибридная терапия», сочетающая катетерное вмешательство и последующее медикаментозное лечение. В случае рецидива ФП может быть выполнена повторная баллонная криоаблация или радиочастотная катетерная аблация.