Транзиторное повышение активности печеночных трансаминаз что это такое
Транзиторное повышение активности печеночных трансаминаз что это такое
Ознакомьтесь, пожалуйста, с правилами использования информации, размещенной в этом разделе сайта.
В соответствии с положениями Федерального закона «Об обращении лекарственных средств» от 12 апреля 2010 года № 61-ФЗ информация, размещенная на данном разделе сайта, квалифицируется как информация о лекарственных препаратах, отпускаемых по рецепту. Данная информация представляет собой дословные тексты и цитаты монографий, справочников научных статей, докладов на конгрессах, конференциях, симпозиумах, научных советов, а также инструкций по медицинскому применению лекарственных средств, производимых фармацевтической компанией «ПРО.МЕД.ЦС Прага а.о. (Чехия).
В соответствии с действующим законодательством Российской Федерации данная информация предназначена исключительно для медицинских и фармацевтических работников и может быть использована только ими.
Ничто в данной информации не может рассматриваться в качестве рекомендации гражданину (пациенту) по диагностированию и лечению каких-либо заболеваний и не может служить для него заменой консультации с медицинским работником.
Ничто в данной информации не должно быть истолковано как обращенный к гражданину (пациенту) призыв самостоятельно приобретать или применять какое-либо из вышеуказанных лекарственных средств.
Данная информация не может быть использована гражданином (пациентом) для самостоятельного принятия им решения о медицинском применении какого-либо из вышеуказанных лекарственных средств и/или решения об изменении рекомендованного медицинским работником порядка медицинского применения какого-либо из вышеуказанных лекарственных средств.
Данная информация относится только к лекарственным средствам, зарегистрированным в Российской Федерации в установленном законом порядке. Названия вышеуказанных лекарственных средств, зарегистрированных в других странах, а также рекомендации по их медицинскому применению могут отличаться от информации, размещенной в этом разделе сайта. Не все вышеуказанные лекарственные средства, находящиеся в обращении на территории Российской Федерации, являются разрешенными к медицинскому применению в других странах.
Архив
Интерпретация незначительно повышенного
уровня печеночных трансаминаз
у бессимптомного пациента 1
Paul T. Giboney
Am Fam Physician 2005;71:1105-10
Определение уровня печеночных трансаминаз — аланинтрансаминазы (АЛТ) и аспартаттрансаминазы (АСТ) — часто входит в перечень стандартных лабораторных исследований бессимптомных амбулаторных пациентов, подобно скрининговым тестам для доноров крови и лиц, желающих застраховать свою жизнь. Поэтому семейным врачам часто приходится обследовать бессимптомных пациентов с повышенным уровнем АЛТ или АСТ.
У около 4% бессимптомных пациентов имеют место патологиеские результаты биохимических печеночных проб, в частности повышение уровней трансаминаз в сыворотке крови.
По данным Американской гастроэнтерологической ассоциации (АГА), у 1–4% бессимптомных пациентов отмечается повышение содержания печеночных ферментов в сыворотке крови. Приведенные данные совпадают с общепринятым определением повышенного уровня трансаминаз — на 2,5% выше уровней в популяции. Хотя во время обследования 19 877 бессимптомных молодых курсантов Военно-воздушных сил (в 1993 г.) только у 0,5% из них был обнаружен повышенный уровень АЛТ, врачи, у которых больше больных с ожирением, диабетом и гиперлипидемией, будут чаще сталкиваться с данной ситуацией.
Маркеры поражения и некроза печени
АЛТ и АСТ — наиболее достоверные маркеры поражения и некроза печени. АЛТ считается более специфичным для заболеваний печени, поскольку данный фермент преимущественно содержится в ее цитозоле. Различают цитозольную и митохондриальную изоформы АСТ, находящиеся в печени, сердце, скелетных мышцах, почках, головном мозге, поджелудочной железе, легких, лейкоцитах и эритроцитах.
Хотя уровень АЛТ и АСТ может быть резко повышенным (превышать 2000 ед./л при повреждении гепатоцитов в результате ишемии, гепатита, воздействия лекарств или токсинов), в практике семейного врача намного чаще встречаются показатели, превышающие верхнюю границу нормы менее чем в 5 раз (то есть 2 повышения АЛТ или АСТ (по D. S. Pratt, M. M. Kaplan, 2000)
Наиболее частые печеночные факторы
• Хронический гепатит В или С
• Острый вирусный гепатит
Редко встречающиеся печеночные факторы
• Избыточные физические нагрузки
Соотношение АСТ/АЛТ имеет определенное клиническое значение, но также и важные ограничения. При многих формах острого и хронического повреждения печени или стеатоза данный показатель не превышает 1, что в особенности касается больных с гепатитом С. Тем не менее для алкогольного гепатита характерный коэффициент АСТ/АЛТ более 2. Во время недавнего исследования (Pratt D. S., Kaplan M. M., 2000) 140 пациентов с неалкогольным стеатогепатитом (НАСГ), подтвержденным биопсией печени, или алкогольным поражением печени (АПП) было установлено, что коэффициент АСТ/АЛТ составлял в среднем 0,9 при НАСГ и 2,6 — при АПП. В пределах исследованной популяции у 87% больных с коэффициентом АСТ/АЛТ ≤ 1,3 был обнаружен НАСГ (чувствительность 87%, специфичность 84%). Тяжесть НАСГ (определялась по степени фиброза) возрастала по мере повышения коэффициента АСТ/АЛТ. При циррозе, связанном с НАСГ, средний коэффициент АСТ/АЛТ составлял 1,4, а при болезни Вильсона — мог превышать 4. Хотя величина данного коэффициента помогает заподозрить определенный диагноз, слишком часто наблюдаются совпадения между различными группами пациентов, чтобы диагноз основывался исключительно на его значении.
Лактатдегидрогеназа (ЛДГ) — менее специфичный маркер гепатоцеллюлярного некроза, он обычно не дополняет диагностическую информацию, полученную при определении уровней АЛТ и АСТ, за исключением временного, но выраженного повышения уровня ЛДГ при ишемическом гепатите и сохранения его возросшей концентрации, которая наряду с возрастанием уровня щелочной фосфатазы свидетельствует об инфильтрации печени злокачественными клетками.
АЛТ считается более специфическим для заболеваний печени, поскольку данный фермент в основном содержится в цитозоле печени и в низких концентрациях — в других органах.
Повышение уровня АСТ и АЛТ наблюдается не только исключительно при печеночной патологии. Несколько исследований (Bayraktar M. et al., 1997) подтвердили, что гипертиреоз может приводить к повышению уровней печеночных ферментов в сыворотке крови, в том числе АСТ и АСТ. На уровень АЛТ также могут влиять генетические факторы. Во время исследования датской двойни (Bathum L., 2001) было доказано, что у пациентов в возрасте 73–94 лет 33–66% случаев колебаний уровня АЛТ, γ-глютамилтранспептидазы, ЛДГ и билирубина в сыворотке крови предопределялось генетическими факторами. В техническом обзоре АГА подчеркивается, что уровень АЛТ может изменяться на протяжении суток, изо дня в день и под воздействием физической нагрузки, а уровень АСТ у темнокожих людей может быть на 15% выше, чем у белого населения.
Еще одним этиологическим фактором повышения уровня трансаминаз является повреждение мышц. Избыточная физическая нагрузка или миопатия могут приводить к их повышению (особенно АСТ) при отсутствии какой-либо другой симптоматики. Для подтверждения следует определить уровень креатининкиназы или другого маркера повреждения мышц.
Ежегодный скрининг здоровых, бессимптомных лиц на предмет наличия заболеваний печени путем определения уровня АЛТ и АСТ нецелесообразен. Во время японского исследования (Yano E. et al., 2001) у работников банков мужского пола определялись уровни АЛТ и АСТ с целью диагностики гепатита С, чрезмерного употребления алкоголя и жирового гепатоза, однако чувствительность метода оказалась низкой. Только у 3,9% мужчин с патологическим уровнем АЛТ был обнаружен гепатит С, у 8% — результаты свидетельствовали о чрезмерном употреблении алкоголя, а у 35,7% имел место жировой гепатоз.
Критическим вопросом обследования больных с незначительно повышенным уровнем печеночных трансаминаз является тщательный сбор анамнеза и физикальное обследование. Из анамнеза следует попытаться узнать о факторах риска заболеваний печени, обращая особое внимание на семейный анамнез, прием лекарств, витаминов, растительных добавок, наркотиков, алкоголя, трансфузии препаратов крови, патологические результаты печеночных проб в прошлом и симптоматику заболеваний печени. В таблице 2 перечислены медикаменты и растительные добавки, способные приводить к повышению уровней трансаминаз. Врачу следует прямо спросить больного об употреблении запрещенных препаратов, растительных и других альтернативных добавок, поскольку вначале он может о них промолчать.
Таблица 2. Наиболее частые средства, приводящие к повышению уровней печеночных трансаминаз (по Pratt D. S., Kaplan M. M., 2000)
Повышена гамма-ГТ: причины, что значит и о чем говорит
Гамма-ГТ — фермент, который участвует в процессе обмена кислот, оттока желчи. При повышении показателей возникают проблемы с пищеварением, воспаления различных внутренних органов. Уровень гамма-ГТ в крови определяют при помощи биохимического анализа.
Что такое Гамма-ГТ, нормы показателей для мужчин и женщин?
ГТГ — гамма глютамилтрансфераза, фермент который содержится в цитоплазме и лизосомах головного мозга, печени, почек, селезенки и поджелудочной железы, простаты. Если клетки этих органов разрушаются, фермент проникает в системный кровоток, повышается его концентрация в крови.
При каких симптомах назначают анализ на ГТГ?
Биохимический анализ крови для определения уровня гамма-ГТ может назначить терапевт, кардиолог, гастроэнтеролог при наличии следующих жалоб:
Диагностику проводят для выявления заболеваний печени, отслеживания динамики при инфаркте миокарда, циррозе, хронических гепатитах, раке поджелудочной железы. Анализ назначают людям с алкогольной зависимостью, для оценки воздействия некоторых лекарственных препаратов на печень.
Кровь для определения уровня гамма-ГТ берут из вены. За 48 часов до анализа нужно исключить из рациона жирную, соленую, жареную, тяжелую, пряную пищу. За 12 часов до забора биоматериала необходимо исключить физические нагрузки, не употреблять спиртные напитки, избегать стрессов, не посещать сауну и баню. Кровь нужно сдавать натощак, последний прием пищи — за 12 часов до обследования. Утром можно пить только чистую воду.
При каких патологиях повышаются показатели гамма-ГТ?
Увеличение концентрации ГТГ в крови может быть признаком следующих заболеваний:
Тест на ГТГ — один из самых чувствительных анализов для выявления застоя желчи. При холестазе показатели фермента повышаются раньше, чем возникает активность щелочной фосфатазы. Чем выше активность ГТГ, тем сильнее повреждена печень или желчевыводящие ходы. При опухолях печени, остром гепатите и холангите, алкогольной интоксикации, закупорке желчных протоков значения возрастают более, чем в 10 раз. При хроническом гепатите, циррозе и болезнях желчного пузыря — в 5-10 раз.
Высокие показатели гамма-ГТ наблюдаются у людей с лишним весом, алкогольной зависимостью, во время беременности. Концентрация фермента возрастает при длительном приеме противозачаточных таблеток, антибиотиков, противомикробных средств, антидепрессантов, препаратов для стимуляции синтеза тестостерона. Активность ГТГ возрастает при приеме медикаментов с ацетилсалициловой кислотой, парацетамолом, лекарств для снижения уровня холестерина, препаратов для лечения эпилепсии или туберкулеза.
Снижение показателей ГТГ наблюдается при гипотиреозе — снижении функций щитовидной железы, при декомпенсированном циррозе печени, при длительном приеме аскорбиновой кислоты.
Как нормализовать показатели?
Чтобы снизить уровень ГТГ, необходимо вылечить основное заболевание, прекратить прием медикаментов-индукторов, алкоголя.
Какие препараты может назначить врач:
Диета при высоком уровне ГТГ
Диетотерапия — одна из важных составляющих при лечении болезней печени, желчевыводящих путей. Для снижения показателей ГТГ нужно питаться дробно — принимать пищу 5-6 раз в день небольшими порциями. Последний прием пищи за 2 часа до сна. Суточная норма углеводов — 350-400 г, при этом быстрых углеводов должно быть не более 70 г. В день выпивать до 1,5 л жидкости.
Продукты мелко нарезать или измельчать в блендере. Блюда готовить на пару, запекать, варить. Пища должна быть средней температуры — 15-65 градусов, горячая и холодная еда стимулирует синтез желчи.
Разрешенные блюда и продукты:
Из рациона необходимо исключить жирные блюда, фастфуд, ограничить количество соли до 10 г в день. Полностью противопоказаны алкогольные и газированные напитки, пряности, любые кислые овощи, фрукты, копчености, консервы, колбасные изделия, какао.
Патологии печени, желчевыводящих путей могут долгое время протекать без выраженных симптомов. Боль, диспепсические расстройства часто появляется при запущенных формах болезни. Чтобы снизить риск развития заболеваний, необходимо отказаться от вредных привычек, правильно питаться, регулярно проходить профилактические осмотры.
Интерпретация биохимического анализа крови при патологии печени. Синдром цитолиза. Часть 1.
Опубликовано в журнале:
«Практика педиатра» июнь, 2017г.
М. Г. Ипатова 1, 2 к.м.н., Ю. Г. Мухина 1 д.м.н. профессор, П. В. Шумилов 1 д.м.н., профессор
1 Российский национальный исследовательский медицинский университет им. Н. И. Пирогова
МЗ РФ, Москва
2 Детская Городская Клиническая Больница № 13 им. Н. Ф. Филатова, Москва
Ключевые слова: печень, синдром цитолиза, аланинаминотрансфераза, аспартатамино—трансфераза, гепатопротективные препараты
В статье изложены биохимические лабораторные показатели и их клиническое значение при заболеваниях печени, протекающих с синдромом цитолиза. Отдельное внимание уделено механизмам действия гепатопротективных препаратов, применяемых при цитолитическом синдроме.
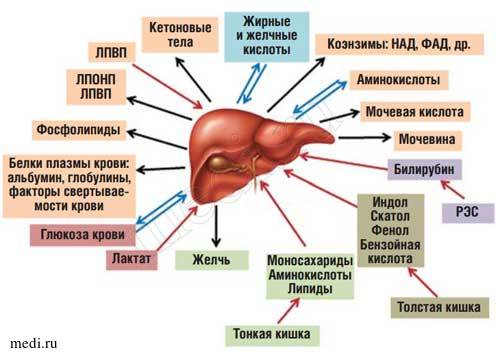
Рис. 1. Роль печени в обмене веществ.
Печень представляет собой центральный орган химического гомеостаза организма, где создается единый обменный и энергетический пул для метаболизма почти всех классов веществ [1]. К основным функциям печени относятся: метаболическая, депонирующая, барьерная, экскреторная, гомеостатическая и детоксицирующая [2]. Печень может обезвреживать как чужеродные экзогенные вещества, обладающие токсическими свойствами, так и синтезированные эндогенно.
Таблица 2. Причины повышения уровня аминотрансфераз
Печеночные причины
Внепеченочные причины
•Вирусные гепатиты (В, С, ЦМВ и др.)
•Хронические инфекции и паразитарные
заболевания (эхинококкоз, токсоплазмоз и др.)
•Неалкогольный стеатогепатит
•Аутоиммунные заболевания печени
•Злоупотребление алкоголем
•Прием лекарственных препаратов
(статины, некоторые антибиотики, противогрибковые препараты, нестероидные
противовоспалительные препараты,
глюкокортикостероиды, другие)
•Метаболические заболевания печени
(галактоземия, фруктоземия, гликогенозы,
дефицит альфа1-антитрипсина,
аминоацидопатии, нарушение цикла мочевины, нарушение окисления жирных кислот, митохондриальная гепатопатия, некоторые лизосомные заболевания (болезнь
Гоше, болезнь Ниманна-Пика, дефицит кислой липазы и др.), муковисцидоз, синдром Швахмана-Даймонда, гемохроматоз, болезнь Вильсона и др.)
•врожденные и приобретенные дефекты
сосудов системы воротной вены (болезнь
Бадда-Киари и др.)
•Цирроз печени
•Опухоли печени
•Патология сердца (острый инфаркт
миокарда, миокардит)
•Повышенная физическая нагрузка
•Наследственные нарушения мышечного
метаболизма
•Приобретенные мышечные заболевания
•Травма и некроз мышц
•Целиакия
•Гипертиреоз
•Тяжелые ожоги
•Гемолиз эритроцитов
•Нарушение кислотно-щелочного равновесия
•Сепсис
Находясь между портальным и большим кругами кровообращения, печень выполняет функцию большого биофильтра. Через воротную вену в нее поступает более 70% крови, остальная кровь попадает через печеночную артерию. Большая часть веществ, всасывающихся в пищеварительном тракте (кроме липидов, транспорт которых в основном осуществляется через лимфатическую систему), поступает по воротной вене в печень [2]. Таким образом, печень функционирует как первичный регулятор содержания в крови веществ, поступающих в организм с пищей (рис 1).
Большое разнообразие функций гепатоцитов приводит к тому, что при патологических состояниях печени нарушаются биохимические константы, отражающие изменения многих видов обмена. Поэтому стандартный биохимический анализ крови включает определение различных параметров, отражающих состояние белкового, углеводного, липидного и минерального обмена, а также активность некоторых ключевых ферментов.
Концентрация ферментов в клетках значительно выше, чем в плазме крови; в норме только очень незначительная часть определяется в крови. Наиболее частыми причинами повышения уровня ферментов в сыворотке крови являются: прямое поражение клеточных мембран, в частности вирусами и химическими соединениями, гипоксия и ишемия тканей. Иногда активность ферментов увеличивается в результате их повышенного синтеза в тканях. Определение активности тех или других ферментов в сыворотке крови позволяет судить о характере и глубине поражения различных компонентов гепатоцитов [3, 4].
Ферменты в зависимости от их локализации можно разделить на несколько групп:
1) универсально распространенные ферменты, активность которых обнаруживается не только в печени, но и в других органах – амино-трансферазы, фруктозо-1-6-дифосфатальдолаза;
2) печеночноспецифические (органоспе-цифические) ферменты; их активность исключительно или наиболее высоко выявляется в печени. К ним относятся холинэстераза, орнитин-карбамилтрансфераза, сорбитдегидрогеназа и др.;
3) клеточноспецифические ферменты печени относят преимущественно к гепатоцитам,
купферовским клеткам или желчным канальцам (5-нуклеотидаза, аденозинтрифосфатаза);
4) органеллоспецифические ферменты, являются маркерами определенных органелл
гепатоцита: митохондриальные (глутаматде-гидрогеназа, сукцинатдегидрогеназа, цитохромоксидаза), лизосомальные (кислая фос фатаза, дезоксирибонуклеаза, рибонуклеаза), микросомальные (глюкозо-6-фосфатаза).
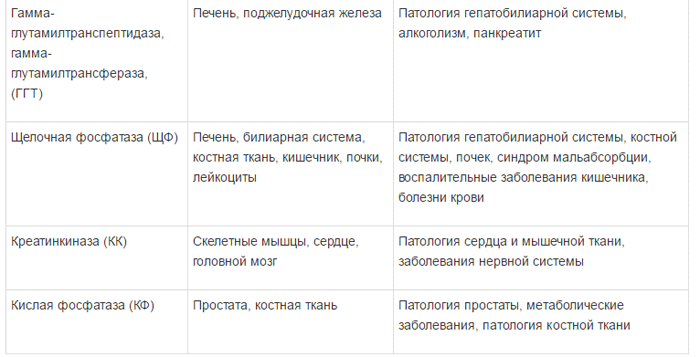
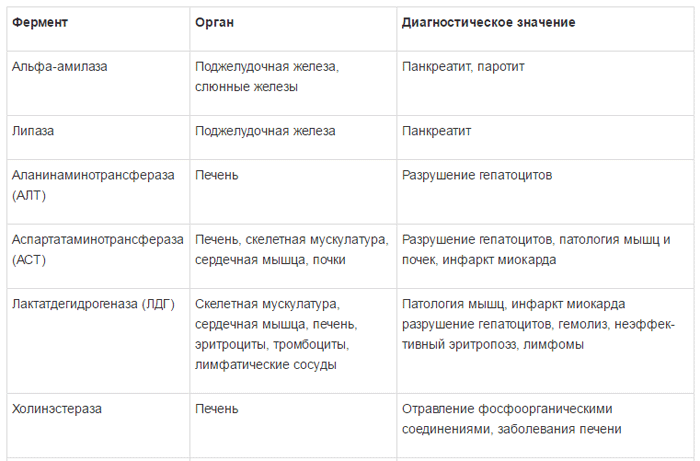
Специфичность ферментов и их диагностическое значение представлено в таблице 1 [5].
Исходя из выше изложенного, следует, что в большинстве случаев отклонения активности сывороточных ферментов от «нормы» неспецифичны и могут быть вызваны различными причинами. Поэтому нужно с большой осторожностью относиться к интерпретации этих отклонений, сопоставляя их с клинической картиной заболевания и данными других лабораторных и инструментальных методов исследования [5, 6].
В связи с использованием в клинических лабораториях разных методов исследования ферментов и единиц измерения их активности целесообразно каждый раз, получив результаты анализа, уточнить, каким методом и в каких единицах была измерена активность фермента, и сопоставить полученное значение с «нормой», принятой в данной лаборатории.
Отдельное место занимает макроэнзиме-мия – редкое и крайне сложное для дифференциальной диагностики состояние, при котором происходит комплексирование молекул того или иного энзима с иммуноглобулинами или небелковыми веществами. Описаны клинические наблюдения макро-КФК-емии, макро-ЛДГ-емии, макро-АСТ-емии, макро-ГГТ-емии, макроамилаземии. Макро-энзимемии сложны для диагностики и дифференциальной диагностики и ведут к проведению инвазивных методов обследования и необоснованному лечению.
В основе выявления макроэнзимемии лежит выявление отличий молекулы макрофермента от молекулы обычного энзима. Некоторые из этих методов являются прямыми, т. е. такими, которые позволяют непосредственно определить присутствие в крови ферментного комплекса, имеющего гораздо более высокий молекулярный вес, чем молекула нормального фермента. В основу прямого метода положено разделение белков сыворотки по молекулярному весу. Другие же методы являются непрямыми, так как выявление макроэнзима в крови проводится не путем выявления самого ферментного комплекса, а основываются на выявлении какого-либо из свойств макроэнзима. Прямые тесты имеют большее диагностическое значение и влекут за собой меньше технических и диагностических ошибок.
В некоторых ситуациях повышение ферментов является физиологическим: уровень щелочной фосфатазы повышен у подростков в период вытяжения (период ускорения роста), у здоровых женщин во время третьего триместра беременности (за счет плаценты). Однако очень высокую активность щелочной фосфатазы наблюдают у женщин с преэк-лампсией, что связно с нарушением кровообращения плаценты [7].
Большое значение в диагностике заболеваний печени имеют анамнестические данные и клиническая картина заболевания. Из анамнеза следует попытаться узнать о факторах риска заболеваний печени, обращая особое внимание на семейный анамнез, прием лекарств, витаминов, растительных добавок, наркотиков, алкоголя, трансфузии препаратов крови, патологические результаты печеночных проб в прошлом и симптоматику заболеваний печени. Клиническое обследование позволяет диагностировать до 50–60% патологических состояний. Более детальная дифференциальная диагностика основана на иммунохимических методах. Они позволяют детализировать характер вирусной, а также паразитарной инфекции, определить локализацию неопластического процесса, определить этиологию аутоиммунного заболевания, уточнить вид нарушения наследственных заболеваний обмена веществ.
При патологии печени в биохимическом анализе крови выделяют 4 синдрома:
• Синдром печеночно-клеточной недостаточности
• Мезенхиально-воспалительный синдром.
В данной статье мы подробно разберем по
казатели, характерные для синдрома цитолиза.
Синдром цитолиза – это синдром, обусловленный нарушением проницаемости клеточных мембран, распадом мембранных структур или некрозом гепатоцитов с выходом в плазму ферментов (АЛТ, АСТ, ЛДГ, альдолазы и др.).
АМИНОТРАНСФЕРАЗЫ: аспартатаминотрансфераза и аланинаминотрансфераза
Референтные значения: у новорожденных детей до 1 мес. – менее 80 Ед/л; от 2 мес. до 12 мес. – менее 70 Ед/л., с 1 года до 14 лет – менее 45 Ед/л, у женщин – менее 35 Ед/л, у мужчин – менее 50 Ед/л.
В клинической практике широко применяется одновременное определение уровня двух трансаминаз – аспартатаминотрансферазы (AСT) и аланинаминотрансферазы (АЛТ) в сыворотке крови.
Ферменты АЛТ и АСТ содержатся практически во всех клетках человеческого организма. Однако самый высокий уровень фермента АЛТ содержится в печени, поэтому уровень данного энзима служит специфическим маркером поражения печени. В свою очередь, АСТ помимо печени (в порядке снижения концентрации) содержится в сердечной и скелетных мышцах, почках, поджелудочной железе, легких, лейкоцитах и эритроцитах [6, 7, 8].
В печени АЛТ присутствует только в цитоплазме гепатоцитов, а АСТ – в цитоплазме и в митохондриях. Более 80% печеночной АСТ представлено именно митохондриальной фракцией [6, 7, 8].
В норме постоянство концентрации транс-аминаз в плазме крови отражает равновесие между их высвобождением вследствие физиологического апоптоза состарившихся гепатоци-тов и элиминацией. Соотношение синтеза АСТ/ АЛТ в печени равно 2,5/1. Однако при нормальном обновлении гепатоцитов уровни АСТ и АЛТ в плазме крови практически одинаковы (30–40 Ед/л) из-за более короткого периода полувыведения АСТ (18 ч против 36 ч у АЛТ).
При заболеваниях печени в первую очередь и наиболее значительно повышается активность АЛТ по сравнению с АСТ. Например, при остром гепатите, независимо от его этиологии, активность аминотрансфераз повышается у всех больных, однако преобладает уровень АЛТ, содержащейся в цитоплазме, вследствие ее быстрого выхода из клетки и поступления в кровяное русло. Таким образом, по уровню АЛТ судят о биохимической активности заболевания печени. Повышение показателя в 1,5–5 раз от верхней границы нормы свидетельствует о низкой активности процесса, в 6–10 раз – об умеренной и более 10 раз – о высокой биохимической активности. Повышение активности трансаминаз более 6 месяцев является биохимическим признаком хронического гепатита [6, 7].
Некоторые лекарственные препараты (например, вальпроевая кислота) метаболизируются в митохондриях гепатоцитов [9], поэтому ранним лабораторным маркером гепатотоксичности может быть лишь изолированное повышение АСТ.
Помимо патологии печени АСТ служит одним из ранних маркеров повреждения сердечной мышцы (повышается у 93–98% больных инфарктом миокарда до 2–20 норм); специфичность его не высока. Уровень ACT в сыворотке крови возрастает через 6–8 часов после начала болевого приступа, пик приходится на 18–24 часа, активность снижается до нормальных значений на 4–5 день. Нарастание активности фермента в динамике может свидетельствовать о расширении очага некроза, вовлечении в патологический процесс других органов и тканей, например, печени [7].
Интенсивные мышечные упражнения с чрезмерной нагрузкой также могут вызвать преходящее увеличение уровня ACT в сыворотке крови. Миопатии, дерматомиозиты и другие заболевания мышечной ткани вызывают повышение трансаминаз, преимущественно за счет АСТ.
Умеренное увеличение активности АСТ (в 2–5 раз от верхней границы нормы) отмечается при острых панкреатитах и гемолитических анемиях.
При латентных формах цирроза печени повышения активности ферментов, как правило, не наблюдают. При активных формах цирроза стойкий незначительный подъем аминотрансфераз выявляют в 74–77% случаев, и, как правило, преобладает активность АСТ над АЛТ в два и более раз.
Снижение активности АЛТ и АСТ имеет место при недостаточности пиридоксина (витамина В6), при почечной недостаточности, беременности.
Ниже приведены печеночные и внепеченочные причины повышения активности аминотрансфераз в сыворотке крови (табл. 2).
Помимо оценки уровня трансаминаз в клинической практике широко применяется коэффициент де Ритиса – отношение АСТ к АЛТ (АСТ/АЛТ). В норме значение этого кэффициента составляет 0,8–1,33. Следует отметить, что расчет коэффициента де Ритиса целесообразен только при выходе АСТ и/или АЛТ за пределы референтных значений.
У новорожденных детей соотношение АСТ/АЛТ обычно превышает 3,0, однако к пятому дню жизни снижается до 2,0 и ниже.
При поражениях печени с разрушением гепатоцитов преимущественно повышается АЛТ, коэффициент де Ритиса снижается до 0,2–0,5. При патологии сердца преобладает уровень АСТ, и коэффициент де Ритиса повышается. Однако для точной дифференциальной диагностики этот коэффициент непригоден, так как нередко при алкогольном поражении печени, неалкогольном стеатогепатите, циррозе печени также преобладает повышение АСТ и коэффициент де Ритиса составляет 2,0–4,0 и более. Значение данного коэффициента выше нормы часто наблюдается при обтурационных желтухах, холециститах, когда абсолютные значения АЛТ и АСТ невелики.
1. При остром вирусном и хроническом гепатитах, особенно на ранних стадиях, активность АЛТ выше, чем АСТ (коэффициент де Ритиса меньше 1,0). Тяжелое поражение паренхимы печени может изменить это соотношение.
2. При алкогольном гепатите и циррозе нередко активность АСТ оказывается выше, чем АЛТ (коэффициент де Ритиса больше 1,0).
3. При остром ИМ активность АСТ выше, чем АЛТ (коэффициент де Ритиса больше 1,5).
ЛАКТАТДЕГИДРОГЕНАЗА
Референтные значения ЛДГ для новорожденных – до 600 Ед/л, у детей с 1 года до 12 лет активность ЛДГ – 115 – 300 Ед/л, для детей старше 12 лет и у взрослых норма ЛДГ – до 230 Ед/л.
Лактатдегидрогеназа (ЛДГ) – гликолитический цинксодержащий фермент, обратимо катализирующий окисление L-лактата в пируват, широко распространен в организме человека. Наибольшая активность ЛДГ обнаружена в почках, сердечной мышце, скелетной мускулатуре и печени. ЛДГ содержится не только в сыворотке, но и в значительном количестве в эритроцитах, поэтому сыворотка для исследования должна быть без следов гемолиза [7].
При электрофорезе или хроматографии удается обнаружить 5 изоферментов ЛДГ, отличающихся по своим физико-химическим свойствам. Наибольшее значение имеют два изофермента – ЛДГ1 и ЛДГ5. Фракция ЛДГ1 более активно катализирует обратную реакцию превращения лактата в пируват. Она в большей степени локализуется в сердечной мышце и некоторых других тканях, в норме функционирующих в аэробных условиях. В связи с этим миокардиальные клетки, обладающие богатой митохондриальной системой, окисляют в цикле трикарбоновых кислот не только пируват, образующийся в результате протекающего в них самих процесса гликолиза, но и лактат, образующийся в других тканях. Фракция ЛДГ5 более эффективно катализирует прямую реакцию восстановления пирувата в лактат. Она локализуется преимущественно в печени, в скелетных мышцах. Последние нередко вынуждены функционировать в анаэробных условиях (при значительной физической нагрузке и быстро наступающем утомлении). Образующийся при этом лактат с кровотоком попадает в печень, в которой он используется для процесса глюконеогенеза (ресинтеза глюкозы), а также в сердце и другие ткани, где происходит его преобразование в пируват и вовлечение в цикл трикарбоновых кислот (цикл Кребса). Любое повреждение клеток тканей, содержащих большое количество ЛДГ (сердце, скелетные мышцы, печень, эритроциты), приводит к повышению активности ЛДГ и ее изо-ферментов в сыворотке крови. Наиболее частыми причинами повышения активности ЛДГ являются:
1. Поражение сердца (острый инфаркт миокарда, миокардит, застойная сердечная недостаточность); в этих случаях обычно преобладает повышение активности ЛДГ1 и/или ЛДГ2.
2. Поражение печени (острые и хронические гепатиты, цирроз печени, опухоли и метастазы печени), когда преимущественно увеличивается изофермент ЛДГ5, ЛДГ2, ЛДГ4.
3. Повреждение скелетных мышц, воспалительные и дегенеративные заболевания
скелетных мышц (преимущественно увеличение изофермента ЛДГ1, ЛДГ2, ЛДГ3).
4. Заболевания крови, сопровождающиеся распадом клеток крови: острый лейкоз, гемолитическая анемия, В12-дефицитная анемия, серповидноклеточная анемия, а также заболевания и патологические состояния, сопровождающиеся разрушением тромбоцитов (массивная гемотрансфузия, эмболия легочной артерии, шок и др.). В этих случаях может преобладать повышение активности ЛДГ2, ЛДГ3.
5. Острый панкреатит.
6. Заболевания легких (пневмония и др.)
8. Опухоли (повышенный уровень ЛДГ наблюдается в 27% случаев опухолей в I стадии и в 55% – метастатических семином).
Следует помнить, что многие заболевания сердца, скелетных мышц, печени и крови могут сопровождаться повышением активности в сыворотке крови общей ЛДГ без отчетливого преобладания какого-либо из ее изоферментов.
Таблица 3. Эффективность гепатопротекторов при синдроме цитолиза (по С. В. Морозову с соавт., 2011 г. и Н. Б. Губергриц, 2012 г.) [10]