Риск перинатальной потери что это такое
Влияние перинатальных факторов на исход родов у женщин с различной степенью риска
Одной из актуальнейших проблем акушерской науки и практики является снижение перинатальной и материнской смертности. Не вызывает сомнений, что показатели перинатальной смертности и заболеваемости являются производными действия факторов риска, отражающих состояние здоровья матери, течение родов и беременности. Одним из аспектов решения этих проблем является рациональная тактика ведения родов с позиций прогнозирования вероятных осложнений для матери и плода с учетом определения факторов перинатального риска в антенатальном периоде.
В связи с этим целью нашего исследования явилось улучшение исходов беременности и родов у женщин с высоким перинатальным риском путем ранжирования факторов.
Материал и методы. Объектом статистического исследования на различных его этапах явились: женщины родившие путем программированных родов и их новорожденные в период пребывания в родильном доме. Методом сплошной выборки из архива нами были отобраны истории программированных родов женщин наблюдавшихся в отделении дородовой патологии родильного дома № 25 Юго-Западного округа г. Москвы за период с января 2006 года по январь 2007 года.
Для оценки перинатальных факторов риска была использована таблица балльной оценки пренатальных факторов риска, разработанная О.Г. Фроловой и Е.И. Николаевой, незначительно измененная в соответствии с методами данного исследования. Для количественной оценки применялась балльная система. Суммарный подсчет всех имеющихся антенатальных и интранатальных баллов и оценка изменения их проводилось по триместрам (I, II, III). Принципом формирования исследуемых гругтп явилось набранная общая сумма баллов.
Обсуждение. Стратегия риска в акушерстве предусматривает выделение групп женщин, у которых беременность и роды могут осложниться нарушением жизнедеятельности плода, акушерской или экстрагенитальной патологией. Это можно прогнозировать на основании анализа перинатальных факторов риска.
Очень важно понимать, что с прогрессированием беременности изменяется сумма факторов риска в сторону их повышения. Это становится очевидным при проведении балльного скрининга в каждом триместре беременности. Динамическое изменение суммы факторов индивидуально для каждой женщины.
В ходе исследования, суммируя баллы перинатального риска по триместрам, мы наблюдали либо резкий «скачок» их суммы, либо плавный рост и переход беременной из одной группы риска в другую, более неблагоприятную в плане прогнозирования исхода родов.
Суммируя баллы у обследованных женщин, можно сказать, что в первом триместре в группе низкого перинатального риска входило 80% беременных, во втором триместре эта группа уменьшилась до 60%. К концу беременности количество женщин, имеющих низкий перинатальный риск, сокращается еще в два раза.
И еще один аспект проблемы. Беременные средней (не высокой) группы перинатального риска не должны восприниматься медперсоналом как не заслуживающие особого внимания. Наше исследование показало, что частота некоторых осложнений родов выше именно в этой группе, и связано это с недооценкой акушерской ситуации из- за ярлыка «средняя группа риска».
Выводы. Одним из условий благополучного завершения беременности и родов является тщательная оценка и подсчет суммы баллов факторов перинатального риска по триместрам, анализ динамики изменения суммы и коррекция профилактических и лечебных мероприятий.
Беременные с высоким перинатальным риском имеют значительную долю предгравидарных факторов в сумме баллов риска, что откладывает свой отпечаток на течение беременности и родов.
Беременные со средним перинатальным риском накапливают сумму баллов, в основном, в течение беременности за счет ее осложнений.
Беременность «высокого риска» и перинатальные потери
1) ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова» Минздрава России, Санкт-Петербург, Россия;
2) ФГБВОУ ВПО «Военно-медицинская академия имени С.М. Кирова» Министерства обороны России,
Санкт-Петербург, Россия
Цель. Оценка возможности прогнозирования перинатальных потерь с помощью таблицы «Факторы риска во время беременности и в родах».
Материалы и методы. Проведено ретроспективное исследование двух групп, которое включало оценку факторов риска у 664 беременных женщин. В основную группу были включены 307 женщин с перинатальными потерями (159 плодов погибли антенатально, 49 – интранатально, 99 новорожденных погибли в первые 168 ч внеутробной жизни). В контрольную группу вошли 357 (53,8%) женщин без перинатальных потерь. У всех пациенток проведена оценка факторов риска по таблице «Факторы риска во время беременности и в родах» в баллах с дальнейшей оценкой возможности выявления группы высокого риска перинатальной смерти.
Результаты. Анализ балльной оценки социально-биологических факторов, акушерско-гинекологического анамнеза, экстрагенитальной патологии матери не выявил статистически значимых различий в группах сравнения. Построенная методом логистической регрессии математическая модель прогноза вероятности перинатальных потерь обладает высокой специфичностью (более 80%), низкой чувствительностью (40–60%).
Заключение. По данным нашего исследования, таблица «Факторы риска во время беременности и в родах» не может быть использована для прогнозирования перинатальных потерь, так как изначально создавалась для решения другой задачи – определения группы риска. Для прогноза вероятности перинатальной смерти необходимо создание новой прогностической модели с более высокой чувствительностью и достаточной специфичностью, основанной на статистически значимых факторах.
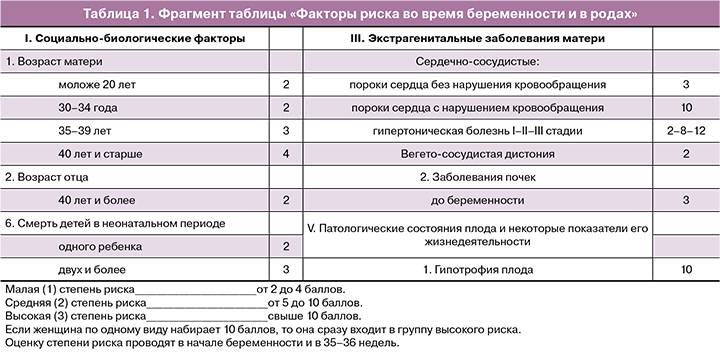
Частота перинатальной смертности в Российской Федерации (РФ) за последние 10 лет имела отчетливую тенденцию к снижению, составив в 2016 г. рекордно низкие 7,34‰, затем несколько увеличилась в 2017 г. до 7,5‰. Однако в ряде субъектов РФ (Брянской, Новгородской, Вологодской областях, республиках Ингушетия, Марий Эл, Забайкальском и Хабаровском краях, Еврейской автономной области и в Чукотском автономном округе) показатель превышает 10‰ [1]. В течение многих лет в РФ существует понятие «беременность высокого риска», связанное и с перинатальными потерями, и с материнской смертностью [2]. Социальный статус, анамнестические данные, течение беременности – все эти показатели входят в таблицу «Факторы риска во время беременности и в родах» (табл. 1), которыми активно пользуются врачи акушеры-гинекологи женских консультаций, заполняя специальные бланки в обменной карте (ф. №113/У). Использование шкалы «Оценка пренатальных факторов риска в баллах» для количественной оценки факторов риска было впервые регламентировано Приказом №430 МЗ СССР от 22.04.1981 г., в дальнейшем пренатальные факторы риска были перечислены в Приказе №50 МЗ РФ от 10.02.2002 г. Таблица предназначена выявлять группу беременных высокого риска. Одним из вариантов крайне неблагоприятного исхода при беременности является перинатальная гибель плода. Мы проанализировали возможность прогнозирования именно перинатальных потерь с использованием таблицы «Факторы риска во время беременности и в родах».
Цель исследования – оценка возможности прогнозирования перинатальных потерь с помощью таблицы «Факторы риска во время беременности и в родах».
Материалы и методы
Проведено ретроспективное исследование двух групп, которое включало комплексный анализ течения беременности у 664 беременных женщин, родоразрешенных в родильных домах г. Санкт-Петербурга и Ленинградской области в 2009–2016 гг. В основную группу были включены 307 женщин с перинатальной гибелью плода (159 плодов погибли антенатально, 49 плодов – интранатально, 99 новорожденных погибли в первые 168 ч внеутробной жизни). В контрольную группу вошли 357 женщин без перинатальных потерь.
Ретроспективный анализ проводили на основании данных обменной карты (ф. №113/У) или истории родов (для родильниц, не состоявших на учете в женской консультации). Контроль перинатальных потерь у родильниц, выписавшихся из родовспомогательного учреждения на 3–5-е сутки, проводили методом телефонного опроса состояния ребенка. Критерии исключения из исследования: многоплодная беременность, невозможность оценки факторов риска из-за отсутствия данных. Для всех пациенток заполнена стандартная таблица «Факторы риска во время беременности и в родах» с последующим подсчетом баллов. Дальнейший анализ проводили с учетом только балльной оценки: средние показатели у каждой пациентки, частота встречаемости в основной и контрольной группе и т.д. не учитывались. Каждому параметру (заболеванию) было присвоено именно то количество баллов, которое было предусмотрено таблицей.
Размер выборки предварительно не рассчитывали. Статистический анализ полученных данных осуществляли с использованием программы STATISTICA 7.0 (Statsoft Inc., США). Количественные данные представлены в виде средних значений и стандартного отклонения. Для проведения анализа количественных данных использовали критерий Манна–Уитни для независимых групп. Для оценки связи качественных показателей рассчитывались таблицы сопряженности и на их основе – χ2 Пирсона. Критерием статистической значимости полученных результатов считали общепринятую в медицинской статистике величину p
Перинатальная потеря: жизнь, которая не успела начаться
Как пережить сильнейшее горе – перинатальную потерю.
Перестала быть беременной, но не стала матерью
Перинатальная потеря – переживание смерти ребенка в утробе матери (антенатальная гибель), процессе родов (интранатальная гибель), в первые семь суток после рождения (ранняя неонатальная гибель), а также переживания аборта, выкидыша, внематочной беременности, замершей беременности.
Скорбь по умершему ребенку является одним из самых сильных и длительных переживаний в жизни человека, тогда как общество подобную утрату не признает и предпочитает замалчивать, оставляя семью наедине со своим горем. До перинатальной утраты у каждой семьи были мечты, надежды, фантазии и стремления, которые рассыпаются вмиг, как карточный домик, оставляя обезумевших от страха родителей наедине с неизвестностью.
Несмотря на факт констатации внутриутробной гибели, женщине необходимо пройти процесс родов в соответствии с утвержденными протоколами. Зачастую персонал роддома действует быстро, применяя тактику экстренного родоразрешения из-за проблемы сепсиса и психологического здоровья роженицы. Молчаливые акушерки, которые привыкли видеть чудо появления новой жизни, в спешке выполняют свою работу, отводят сострадающий взгляд и стараются оградить от переживаний напутствиями скорого наступления новой жизни.
В зарубежной практике встречаются выжидающие тактики, когда роды происходят самопроизвольно в течении нескольких недель после гибели плода, давая возможность подготовиться к исходу и настроиться на встречу со смертью, выбрать ритуалы прощания.
Если в России данная тема находится в разряде табу, создавая дефицит информации, порождая тревогу и страх, замалчивается и сопровождается наставлениями поскорее начать жить дальше, то зарубежная тактика разительным образом отличается от того, что есть у нас сейчас.
Развитие психологической помощи привело к появлению ритуала прощания. Это дает возможность прочувствовать себя в роли родителя конкретного ребенка, а непосредственное знакомство с ним – помогает сохранить воспоминания, которые являются опорой и поддержкой в такой нелегкий жизненный период.
Возможно нам покажется это диким, некими «танцами на костях», но тактика прощания с мертворожденными младенцами включает в себя религиозные ритуалы, фотосессию новорожденных с родителями на память, создание отпечаток ладошек и ножек ребенка, сохранение волос и всего того, что сбережет чувства горюющих родителей, ведь погибший еще в утробе ребенок приравнивается к любому усопшему близкому и значимому человеку.
«The New York Times» публикует семейные фотосессии с мертворожденными на разных сроках детьми, а также письма родителей с их излиянием переживаний, страха, боли и наставлениями всем тем, кто может оказаться на их месте.
Пронзительная и откровенная (Прим. ред.: не переходите по ссылке, если вы очень эмоциональны) фотосессия «рожденных спать на 25 неделе» от синдрома фето-фетальной трансфузии (СФФТ) Гвен и Клары, созданная «Blessed Touch Photography», вызывает бурю эмоций – от неподдельного страха до восхищения силами этой семьи.
Ведь на широкую публику родители выложили весь процесс – непосредственное появление на свет близнецов, их внешний вид, все свои слезы и боль. Родители находились с девочками несколько часов, омыли, расчесали волосики и переодели их в праздничные платья, сделали снимки со старшей дочерью. На данный момент эти сильные люди ведут кампанию по предупреждению потери беременности, распространяя свою историю и тактику переживания перинатальной потери.
«Не увидев ребенка, семья всю жизнь будет создавать его образ, будет представлять что-то страшное
или тосковать, сожалея, что никогда так и не узнали, как он выглядел»
Конечно, бывают случаи, когда ребенок скончался давно и для того, чтобы не нанести психологическую травму от внешнего вида, малыша закутывают в одеяльце и дают тактильно почувствовать, обнять, попрощаться. Семья может не видеть ребенка целиком, но подержаться за крохотную ладонь и сделать фотографии с мягкой игрушкой, которая является наполнением такой распространённой в зарубежных странах «memory box».
Суть такой коробочки памяти проста – она содержит две одинаковые мягкие игрушки, одну из которых запечатлевают с ребенком на фотографии и оставляют в семье, а вторую хоронят вместе с ним. Эту коробочку в дальнейшем заполняют фотоснимками, письмами со словами любви и всегда возвращаются к ней, как к порталу связи с ребенком.
Стадии переживания утраты и избегание темы перинатальной потери
Люди по-разному проживают горе. С разной скоростью проходят стадии принятия случившегося, но избегание переживаний и горя – одна из стратегий взаимодействия с семьей, потерявшей ребенка, принятой в нашем обществе.
Близкие и друзья хранят молчание и предполагают, что любое упоминание еще больше навредит. Партнеры ищут поддержки друг в друге, но зачастую не находят ее, потому что близкий человек не в ресурсе.
Если женщина готова дать волю своим чувствам и слезам, то мужчина жалеет супругу и злится от того, что беспомощен, ничем не может помочь ей, испытывает чувство вины. Именно поэтому мужская скорбь чаще имеет длительный или отложенный характер.
В столь непростой период психологи советуют открыто и честно разговаривать, выслушивая друг друга, выказывая свои чувства, помогая пережить утрату роли родителя и сохранить супружескую роль.
Незнание стадий переживания утраты, их длительности приводят к тому, что окружающие люди поначалу пытаются оказывать посильную моральную поддержку, но через некоторое время делают это все меньше и меньше.
Выделяют четыре стадии переживания утраты:
I стадия – эмоциональный шок и ступор (не превышает двух недель) – психологическая поддержка должна включать в себя помощь в осознании, принятии реальности утраты ребенка и понимании её необратимости;
II стадия – тоска и гнев (до трех месяцев) – поддержку необходимо выстраивать для облегчения переживания душевной боли, снижения проявлений неконструктивного гнева;
III стадия – дезориентация и страдание (наступает между пятым и девятым месяцами после утраты, может длиться год и более) – эффективной поддержкой является создание новых отношений к утраченному ребенку, принятию мира без него;
IV стадия – реорганизация и разрешение (наступает между восемнадцатым и двадцать четвертым месяцем после утраты) – на заключительной стадии психологической поддержки необходимо помочь найти свое место в мире.
Оказывая поддержку, не нужно делать вид, что ничего страшного не произошло, будто этой беременности и этого ребенка не существовало. Помогите пережить горе в полной мере и не вычеркивайте погибшего из жизни этой семьи.
Необходимо готовиться к тому, что переживания еще долго будут сильными и болезненными, поэтому нельзя торопить события. Нужно дать чувствам идти своим чередом, но не игнорировать их.
Напоследок хочется сказать только одно – пусть тема перинатальной потери никогда не коснется вашей семьи!
Перинатальные потери
Познать счастье родительства мечтают многие пары. Но, к сожалению, не каждая беременность заканчивается рождением долгожданного малыша. Большое количество женщин, обращающиеся за помощью в специализированные медицинские учреждения, в своей жизни сталкивались с перинатальными потерями.

· гибель плода во время беременности;
· неудачи при использовании вспомогательных репродуктивных технологий;
· непроизвольное прерывание беременности на ранних сроках («выкидыш»);
· гибель плода во время беременности после 22-х недель;
· гибель одного из близнецов при многоплодной беременности;
· выявление грубой патологии плода при обследовании, а также рождение ребенка-инвалида.
При наступлении беременности редкая женщина называет жизнь внутри нее «эмбрионом», «плодом», «набором клеток», чаще всего звучит «мой ребенок». Уже на ранних сроках возникают фантазии: каким он будет внешне, когда родится, какую кроватку купить и т.д. Поэтому, когда по тем или иным причинам беременность прерывается, возникает ощущение потери близкого человека. Начинается, так называемая, «работа горя». Этот процесс имеет определенные стадии развития:
I. стадия – эмоциональный шок и ступор. Она обычно длится до двух недель. В этот период женщина не может поверить в произошедшее, надеется, что врачи ошиблись. Зачастую пересдает анализ на бета-ХГЧ, проходит УЗИ у другого врача.
II. стадия – тоски поиска ответов, гнева. Все мысли заняты постигшей утратой. Возникает чувство вины «Наверное, я сделала что-то не так». Возникает желание найти виноватых. Гнев может быть направлен на себя, супруга, близких, медперсонал, врачей и самого Господа Бога.
III. стадия – дезориентации и страдания. Возникает упадок сил, нарушения сна, головные боли, ухудшение памяти и внимания, повышается утомляемость, снижается активность и работоспособность, избегается общение, отчаяние. В этот период происходит осознание утраты, а вслед за этим ощущение пустоты и бессмысленности существования. Растет чувство вины. Некоторые женщины хотят как можно быстрее забеременеть снова, другие заявляют, что никогда не будут пытаться.
IV. стадия – реорганизации и разрешения, выход из кризиса. Постепенно восстанавливаются силы, окончательно принимается факт потери. Боль утраты не проходит, но становится терпимой, позволяет жить дальше.
Период, необходимый для переживания утраты, очень индивидуален и зависит от многих факторов: особенности личности, семейной ситуации, наличия поддержки со стороны, срока гибели и т.д. В среднем требуется один год. Очень важно в это время не сдерживать, не подавлять свои эмоции, не замыкаться в себе, не только женщине, но и несостоявшемуся отцу. Горе нужно прожить. Когда боль от потери перестанет быть острой, можно задумываться о следующих попытках забеременеть.
К сожалению, окружающие люди часто не могут оказать необходимую поддержку. Подбирая неудачные фразы, излишне эмоционально реагируя, лишь «подливают масло в огонь». Приведем небольшой список, что следует и не следует говорить при общении с парой, переживающей утрату.
Если не получается самостоятельно справиться со своими переживаниями, следует обратиться к специалисту, в этом нет ничего стыдного, странного.
Статья составлена на основании методического пособия «Оказание помощи семьям при перинатальных утратах» И.В. Добрякова, Л.М. Фаерберга. Ниже прикрепляем брошюры, которые можно использовать для самопомощи или показать близким, столкнувшимся с потерей беременности.
Синдром потери плода
Основной задачей современного акушерства является снижение числа репродуктивных потерь, и актуальность невынашивания беременности (НБ) не вызывает сомнения, так как является наиболее частым ее осложнением.
Основной задачей современного акушерства является снижение числа репродуктивных потерь, и актуальность невынашивания беременности (НБ) не вызывает сомнения, так как является наиболее частым ее осложнением. Несмотря на достигнутые в последние годы успехи в профилактике и лечении данной патологии, частота НБ остается стабильной и достаточно высокой. Так, по данным разных авторов, она составляет от 2% до 55%, достигая в первом триместре 80% [2, 3, 11, 12, 13]. Отсутствие снижения частоты НБ указывает на трудности, возникающие при ведении этой группы пациенток. С одной стороны, они обусловлены многофакторностью этиологии и патогенетических механизмов заболевания. С другой — несовершенством применяемых диагностических методик и отсутствием адекватного мониторинга осложнений, возникающих во время беременности.
Синдром потери плода — это новый термин, появившийся в последнее время и включающий в себя [4]:
Этиология синдрома потери плода чрезвычайно разнообразна и зависит от многих факторов. Одни из них непосредственно приводят к закладке аномального эмбриона, другие создают неблагоприятные условия для его нормального развития.
Основные причины потерь беременности: генетические, эндокринные нарушения, инфекционно-воспалительные заболевания, иммунологические механизмы и тромбофилии.
Под генетическими факторами чаще подразумевают хромосомные аномалии эмбриона, которые появляются в результате слияния двух родительских клеток с точечными мутациями в хромосомном наборе, возникающими из-за нарушения процесса мейоза.
Около 50% спорадических ранних потерь беременности обусловлены хромосомными дефектами. При проведении исследований материала ранних выкидышей генетические аномалии обнаружены в 82% случаев до 6–7 недель и не менее 70% — до 12 недель беременности [17]. По данным разных авторов [11, 12, 22] в первые 6–7 недель беременности аномальный кариотип имеют 60–75% абортусов, в 12–17 недель — 20–25%, 17–28 недель — только 2–7%. На данном факте основан отказ от «сохраняющей» терапии до 11–12 недель беременности в ряде стран Евросоюза.
В структуре привычного НБ (ПНБ) генетические факторы составляют 3–6%, при этом наибольшее значение приобретают структурные изменения хромосом супружеской пары (в 7% обнаруживаются сбалансированные хромосомные перестройки) [10].
При наличии аберраций эмбриогенез либо вообще невозможен, либо резко нарушается на самых ранних стадиях развития. Это связано со сниженной способностью к делению клеток в целом. При этом возникает резкая диссинхронизация процессов развития зародыша, развития плаценты и индукции дифференциации и миграции клеток. Недостаточное и запоздалое формирование плаценты может приводить к нарушению питания и к гипоксии зародыша, а также — к снижению гормональной продукции плаценты, что может быть дополнительной причиной потери беременности.
В этиологии синдрома потери плода эндокринные нарушения матери составляют от 30% до 78,2%. Эндокринная патология независимо от своего генеза, в конечном счете, реализуется структурно-функциональной недостаточностью желтого тела яичника. Неполноценная лютеиновая фаза может быть обусловлена гипотиреозом, поликистозными яичниками, ожирением, дефицитом массы тела, эндометриозом, хроническим эндометритом, сальпингоофоритом, наличием пороков развития матки и генитальным инфантилизмом.
При этом возникает состояние гипопрогестеронемии, которое обуславливает незавершенную гравидационную трансформацию эндометрия. В патогенезе имеет значение как абсолютное содержание стероидных гормонов в плазме крови, так и морфологическая структура эндометрия как органа-мишени, то есть количество функционально полноценных рецепторов. В этих условиях невозможно осуществление полноценной имплантации, вследствие чего формируется первичная плацентарная недостаточность (ПН), которая выражается в нарушении васкуляризации, формирования хориона и приводит к потере беременности в I триместре. Неполноценная имплантация также часто осложняется развитием гестоза, который в свою очередь приводит к формированию вторичной ПН; несовершенство компенсаторных реакций незрелой плаценты способствует формированию абсолютной ПН. При абсолютной ПН внутриутробная гибель плода происходит во II половине беременности [5]. Кроме того, эстрогенный дефицит яичников и гиперандрогения может реализоваться нарушением фолликулогенеза, поломками в процессе мейоза, перезреванием яйцеклетки и, соответственно, потерей беременности.
Учитывая то, что при эндокринных механизмах потери беременности ключевую роль играет патология эндометрия, лечение целесообразно начинать именно с воздействия на это основополагающее звено благоприятного развития беременности.
Хотя результаты современных исследований [18, 20, 21, 24], касающихся прогестеронотерапии НБ, не подтвердили уменьшение риска самопроизвольного аборта, мертворождаемости или неонатальной гибели у женщин с синдромом потери плода при применении прогестагенов, в России [10] сохраняется тактика гормональной поддержки ранних сроков беременности при подтвержденной эндокринной этиологии НБ.
Целью терапии является нормализация гормонального статуса либо медикаментозная компенсация до показателей, необходимых для вынашивания беременности на прегравидарном этапе. Заместительная гормонотерапия способствует полноценной секреторной трансформации эндометрия, оказывает иммуномодулирующее действие, подавляя реакции отторжения со стороны иммунокомпетентных клеток в эндометрии [10]. В России наиболее используемыми являются препараты Утрожестан и Дюфастон, которые обладают выраженным прогестагенным эффектом и имеют свои особенности: Утрожестан обладает седативным и антиатерогенным эффектом, оказывает токолитическое, антиальдостероновое, антиандрогенное, положительное нейротропное действие, не влияет на углеводный обмен, незаменим у женщин с гиперандрогенией, нарушениями углеводного обмена, сахарным диабетом, метаболическим синдромом, гиперхолестеринемией, с патологией желудочно-кишечного тракта (вагинальная форма).
Дюфастон не имеет андрогенной, эстрогенной и кортикостероидной активности, не вызывает сонливость, активен при пероральном применении, обладает выраженными иммуномодулирующими свойствами, регулирует цитокиновый баланс, наиболее целесообразен у женщин с хроническими воспалительными заболеваниями органов малого таза (ВЗОМТ), в том числе с хроническим эндометритом, у пациенток с совместимостью по системе HLA с супругом, при аутоиммунных нарушениях, а также при вождении беременной автотранспорта, влагалищном дисбиозе, вагините. В соответствии с Российскими рекомендациями [10], начатую гормонотерапию на прегравидарном этапе целесообразно продолжить при наступлении беременности до 12–16 недель. Утрожестан применяется по 300–400 мг до 800 мг в сутки до 12–14 недель беременности. Дюфастон назначают по 10–30 мг до 16 недель беременности [10].
Среди ведущих этиологических факторов синдрома потери плода следует отметить инфекционный. ВЗОМТ одна из актуальных проблем современной гинекологии. В структуре гинекологической патологии ВЗОМТ занимают первое место, и их частота не имеет тенденции к снижению. Последнее десятилетие характеризовалось не только сменой возбудителей генитальной инфекции (на первое место вышли представители условно-патогенной микрофлоры), но и изменением клиники воспалительных процессов (первично-латентное течение, без клинических проявлений). Проблема персистирующей инфекции при НБ сложна и дискутабельна. В настоящее время установлено отсутствие строго определенных микроорганизмов, провоцирующих привычную потерю беременности. Однако, даже в случае отсутствия прямого специфического воздействия инфекционных агентов на плод, морфофункциональные нарушения репродуктивной системы, вызванные персистенцией микроорганизмов в эндометрии, с формированием хронического эндометрита, ведут к нарушению развития эмбриона. Микробиологические и морфологические исследования эндометрия выявили наличие хронического эндометрита и персистенции условно-патогенных бактерий у 67,7% женщин с инфекционным генезом НБ.
При неразвивающейся беременности условно-патогенные микроорганизмы выявлены у 20% пациенток, а вирусно-бактериальные ассоциации — у 70% [5]. По данным литературы, у пациенток с хроническими воспалительными процессами чаще обнаруживают стафилококк (15%); стафилококк в ассоциации с кишечной палочкой (11,7%); этерококки (7,2%); вирус простого герпеса (ВПГ) (20,5%); хламидии (15%); микоплазмы (6,1%); уреаплазмы (6,6%); гарднереллы (12,5%) [8]. Бактериально-вирусная контаминация эндометрия является, как правило, следствием неспособности иммунной системы и неспецифических защитных сил организма (системы комплимента, фагоцитоза) полностью элиминировать инфекционный агент наряду с ограничением его распространения за счет активации Т-лимфоцитов (Т-хелперов, естественных киллеров) и макрофагов.
В результате возникает персистенция микроорганизмов, характеризующаяся привлечением в очаг хронического воспаления мононуклеарных фагоциотов, естественных киллеров, Т-хелперов, синтезирующих различные цитокины. Подобное состояние эндометрия препятствует созданию локальной иммуносупресии в предимплантационный период, необходимой для формирования защитного барьера и предотвращения отторжения наполовину чужеродного плода [10].
Некоторые исследователи ведущим этиологическим фактором хронического эндометрита считают вирусы, особенно в тех случаях, когда у женщины зарегистрирована неразвивающаяся беременность [2, 3, 4, 19]. Многие вирусные инфекции как острого, так и латентного течения способны вызвать в организме развитие тромбофилического состояния вследствие поражения эндотелия сосудов (ВПГ, аденовирус), развитие вторичного антифосфолипидного синдрома и/или иммунологических нарушений [4].
Так, по данным В. М. Сидельниковой [11], частота женщин с ПНБ, имеющих цитомегаловирусную инфекцию (ЦМВИ) и ВПГ, колеблется от 55% до 85%. По результатам наших исследований, наличие различных вариантов течения герпетической инфекции у женщин, перенесших неразвивающуюся беременность, зарегистрировано у 67,6% [14]. Комплекс всех этих изменений нарушает процесс инвазии и развития трофобласта, оказывает прямое и опосредованное эмбриотоксическое действие, приводит к формированию первичной и вторичной ПН, что в конечном итоге заканчивается потерей беременности. Нами была разработана математическая модель прогнозирования неразвивающейся беременности у пациенток с герпетической инфекцией на основании показателей функционального состояния эндотелия и гемостазиограммы, позволяющая с высокой чувствительностью и специфичностью выделить среди пациенток группу женщин высокого риска потери беременности [14].
По данным литературы [5, 8], хронический эндометрит гистологически верифицирован у 62% пациенток с ПНБ и у 83% с неразвивающейся беременностью; при антенатальной гибели плода морфологические проявления воспаления в последе встречаются в 85,01 ± 1,32%, при ранней неонатальной смертности — в 85,71 ± 2,70%. На Международном конгрессе «Контраверсии в акушерстве и гинекологии» (Барселона, 2007) постановили ставить диагноз и лечить хронический эндометрит у всех женщин, перенесших хотя бы одну неразвивающуюся беременность.
В России внутриутробные инфекции занимают от 11% до 45% в структуре перинатальной смертности [13], в том числе при антенатальной гибели плода. В результате проведенных нами морфологических исследований последов группы женщин с клинико-аппаратными маркерами внутриутробной инфекции в 25% случаев был выявлен плацентит, острое нарушение плацентарного кровообращения на фоне хронической компенсированной недостаточности в 42%. У 10% — восходящая инфекция, гнойно-некротический мембранит, 32% — слабо выраженные компенсаторно-приспособительные реакции, соответствующие сроку гестации, 25% — признаки замедленного созревания, 8% — склероз ворсин хориона, многочисленные кальцинаты [15].
Бактериологический анализ плацент у женщин из группы риска по ВУИ показал наличие в 51% бактериальной флоры, которая представлена стрептококками — 28%, стафилококками — 22%, пептострептококками — 50%. В 20% случаев происходит ассоциация представленной флоры с уреаплазмой и герпесвирусной инфекцией; моноинфекция: ВПГ (5,8%), ЦМВ (2,2%), Ureaplasma urealyticum parvo (9,6%) [15].
Для снижения роли инфекционно-воспалительных факторов невынашивания проводится лечение на прегравидарном этапе: 1) антибактериальная терапия во время менструации (строго на основании антибиотикограммы); 2) антимикотики; 3) системная энзимотерапия (Вобэнзим, Флогэнзим); 4) иммуномодуляторы с учетом показателей интерферонового статуса; 5) восстановление нормального биоценоза. При наличии вирусной инфекции (ВПГ) в проведение прегравидарной подготовки необходимо включать противовирусные препараты (ацикловир, валацикловир (Валтрекс), фамцикловир) в лечебном и супрессивном режиме [10]. При часто рецидивирующей вирусной инфекции назначается Валтрекс по 500 мг с сутки длительно от 4–6 месяцев до 1–2 лет (супрессивный режим) [10]. При бессимптомном течении герпетической инфекции и вирусовыделении в период прегравидарной подготовки возможно назначение Валтрекса в супрессивном режиме на 3–4 месяца. При беременности необходим контроль состояния биоценоза влагалища, микробиологический и вирусологический контроль. В I триместре беременности у пациенток с инфекционным генезом невынашивания методом выбора является иммуноглобулинотерапия (10% иммуноглобулин человека нормальный для внутривенного введения по 50 мл в/в через день № 3) [10]. Обязательно в I триместре проводить профилактику ПН (метаболические комплексы, нормализация параметров гемостаза). Во II и III триместрах проводят повторные курсы иммуноглобулинотерапии с одновременным лечением ПН.
Иммунологические механизмы потери беременности. Среди них различают аутоиммунные и аллоиммунные процессы. Аутоиммунные реакции направлены против собственных тканей матери, а плод страдает вторично, либо от реакции материнского организма на аутоантитела, либо от идентичности антигенов, на которые у матери возникли аутоантитела [11].
Примером таких аутоиммунных реакций является системная красная волчанка, миастения, аутоиммунный тиреоидит, антифосфолипидный синдром (АФС). При АФС в крови женщины определяются антифосфолипидные антитела (АФА), препятствующие фосфолипид-зависимой коагуляции, без угнетения активности специфических коагуляционных факторов, клиническое проявление данного процесса заключается в развитии тромбоэмболических состояний, в частности избыточного тромбирования в маточно-плацентарной системе кровообращения. Кроме того, АФА подавляют синтез сосудистого кофактора тромбомодуллина, который синтезируется ворсинами хориона, что вызывает снижение образования сосудов и гипоплазию плаценты [7]. АФА изменяют адгезивные характеристики предимплантационной морулы (заряд); усиливают протромботические механизмы и десинхронизируют процессы фибринолиза и фибринообразования, что приводит к дефектам имплантации и снижению глубины децидуальной инвазии трофобласта. АФА напрямую взаимодействуют с синцитиотрофобластом и цитотрофобластом и ингибируют межклеточное слияние клеток трофобласта. Кроме того, АФА подавляют продукцию хорионического гонадотропина и усиливают тромботические тенденции за счет предоставления матриц для реакций свертывания [7].
Основой лечения АФС является коррекция системы гемостаза антикоагулянтами и антиагрегантами: монотерапия ацетилсалициловой кислотой, монотерапия гепарином натрия, низкомолекулярными гепаринами (НМГ), курсы плазмафереза для удаления волчаночного антикоагулянта.
Примером аллоиммунных воздействий могут служить: гемолитическая болезнь новорожденного в связи с Rh- или АВО-сенсибилизацией; неспособность материнского организма выработать антитела, защищающие плод от ее иммунной системы, вследствие совместимости супругов по системе HLA, повышенное содержание в крови и эндометрии матери естественных киллерных клеток (NK-клеток CD56, CD16).
Основная идея совместимости супругов по системе HLA состоит в том, что при этом в организме женщины не вырабатываются антитела, играющие роль блокирующего фактора, что приводит к неэффективному «камуфляжу» плаценты, отсутствию роста и деления плацентарных клеток и к их гибели. При совместимости супругов более чем по двум антигенам HLA риск потери беременности составляет практически 100% [11].
При несовместимости по системе HLA при беременности показано продолжение начатой в периоде предгестационной подготовки иммунотерапии отцовскими или донорскими лимфоцитами [11]. К настоящему времени, однако, не проведены полноценные контролируемые исследования эффективности применения данной методики, кроме того, количественно не определены возможные осложнения использования лимфоцитотерапии [23]. В качестве альтернативной терапии возможно применение высоких доз иммуноглобулина (Human normal immunoglobulini по 50 мл трижды через день внутривенно капельно через каждые 4 недели) [10].
При избыточном содержании в периферической крови и в эндометрии лимфоцитов с фенотипом CD56 во время беременности происходит их патологическая активация, что приводит к избыточному синтезу ими провоспалительных цитокинов, которые нарушают процесс имплантации и способствуют развитию некроза децидуальной ткани и повреждению желточного мешка [16]. При патологической активации CD19+CD5+ В-лимфоцитов в избыточном количестве начинается продукция аутоантител к гормонам, имеющим важное значение для нормального развития беременности: эстрадиола, прогестерона, хорионического гонадотропина [16]. Следствием этого является недостаточность подготовительных к имплантации реакций в эндометрии и децидуальной ткани. Это выражается в децидуальном воспалении и некрозе, в нарушении образования фибриноида и избыточном отложении фибрина. Отмечаются медленный прирост хорионического гонадотропина человека (ХГЧ), повреждение желточного мешка, субхориальные гематомы [11]. Другими продуктами CD19+CD5+ являются антитела к нейротрансмиттерам (серотониту, энкефалинам, эндорфинам), играющим важную роль в процессе подготовки эндометрия к имплантации [16]. В результате воздействия этих антител затрудняется стимуляция яичников, отмечается истончение эндометрия и ослабление в нем ангиогенеза.
Лечение пациенток с сенсибилизацией к ХГЧ состоит в коррекции тромбофилии НМГ под контролем гемостазиограммы и назначении кортикостероидной терапии в дозах 5–15 мг в сутки в расчете на преднизолон. Лечение должно начинаться в первом триместре беременности, так как пик выработки ХГЧ и, как следствие, антител приходится на первые недели беременности [10].
В настоящее время уделяется большое внимание генетически детерминированным формам тромбофилий [7, 17], которые, подобно АФС, сопровождаются тромбоэмболическими осложнениями при беременности и ведут к потере беременности на любом ее этапе. Генетически обусловленные аномалии свертывающей системы крови могут быть связаны с недостаточностью ингибиторов коагуляции, фибринолитических факторов и избыточным уровнем прокоагулянтных факторов. К наиболее часто встречаемым формам наследственных тромбофилий относят: мутацию метилентетрагидрофолатредуктазы — MTHFR, полиморфизм 677 C->T; мутацию фактора Лейдена — F5, полиморфизм 1691 G->A; протромбина (F2), полиморфизм 20210 G->A; ингибитора активатора плазминогена — PAI-1, полиморфизм 675 5G->4 G.
На начальном, аваскулярном, этапе имплантации, который является наиболее уязвимым к действию неблагоприятных факторов (инфекционные агенты, токсины, антитела и др.), важна полноценность системы гемостаза. В условиях наличия тромбофилий (как наследственных, так и приобретенных) и вызванного ими гипофибринолиза происходит десинхронизация локальных процессов фибринолиза и фибринообразования при имплантации. В такой ситуации протеаз, синтезируемых бластоцистой, становится относительно недостаточно, чтобы разрушить экстрацеллюлярный матрикс в эндометрии и внедриться на достаточную глубину. В дальнейшем развивается микротромбообразование и нарушение микроциркуляции, что играет существенную роль в развитии патологии спиральных артерий и акушерских осложнений, связанных с изменением маточно-плацентарного кровообращения [7].
По результатам анализа факторов риска неэффективности методов экстракорпорального оплодотворения и подсадки эмбриона, в результате наших исследований выявлено, что ведущей причиной преэмбрионических потерь является хронический эндометрит, а эмбрионических — патология системы гемостаза [9].
При наличии врожденных тромбофилий начиная с фертильного цикла и в течение всей беременности проводят лечение НМГ и антиагрегантами. В случае гипергомоцистеинемии — необходимо назначение больших доз фолиевой кислоты и витаминов группы В [10].
Для успешной имплантации плодного яйца и прогрессирования беременности необходимы наличие генетически полноценного эмбриона, адекватного развития эндометрия, готового к рецепции бластоцисты и создание в организме матери локальной иммуносупрессии.
Сразу после выхода бластоцисты в полость матки (4–5 день после оплодотворения) она оказывается в секрете, поступающем из многочисленных устьев эндометриальных желез; бластоциста начинает «молекулярный диалог» с маточным эпителием для достижения максимальной рецептивности с «окном имплантации». Важно подчеркнуть, что свободная бластоциста в течение 1,5–2 суток находится в окружении муцина (Мисс-1) и различных эндометриальных белков, которые защищают от инфекций, других вредных воздействий и осуществляют ее иммунную защиту. Поэтому огромное значение в настоящее время отводится изучению микроокружения зародыша в процессе имплантации. Особое внимание уделяется изучению эндометриальных белков [1, 3, 6].
Альфа-2-микроглобулин фертильности (АМГФ) — белок, выделяемый эпителиоцитами маточных желез уже на 5–6 день после овуляции, то есть к тому моменту, когда при состоявшемся оплодотворении бластоциста попадает в полость матки. АМГФ обладает мощной иммуносупрессивной активностью, обеспечивая локальное подавление иммунного ответа матери на развивающийся эмбрион. АМГФ вызывает увеличение продукции интерлейкина-6 эпителием эндометрия, подавляет активность естественных киллеров, что может влиять на формирование системы мать — плацента — плод. АМГФ рассматривают как показатель функциональной активности маточных желез, как маркер секреторной трансформации эндометрия [1, 6].
В процессе погружения бластоцисты в функциональный слой эндометрия появляется принципиально новый механизм репродукции — цитотрофобластическая инвазия. Клетки цитотрофобласта продуцируют каскад особых цинк-зависимых металлопротеаз, которые «протравливают» дорогу для погружающейся бластоцисты. Темпы и глубина цитотрофобластической инвазии определяются местной пара- и аутокринной регуляцией. Одним из паракринных ингибиторов цитотрофобластической инвазии является плацентарный альфа-микроглобулин (ПАМГ), то есть местный эндометриальный белок, синтезируемый децидуальными клетками промежуточного типа [16].
При неполноценности эндометрия эндокринного генеза, на фоне хронического эндометрита, развивается дефицит продукции АМГФ, что приводит к нарушению метаболических и иммунных взаимоотношений эмбриона с материнским организмом, а снижение продукции ПАМГ способствует нарушению трофобластической инвазии, что ведет к гибели эмбриона. В то же время у пациенток с неразвивающейся беременностью на фоне аутоиммунных и генетических нарушений продукция АМГФ и ПАМГ в эндометрии повышена [3].
Необходимо отметить, что к потерям беременности на разных сроках способствуют различные этиологические факторы. В частности: на сроках гестации 5–6 недель преобладают генетические и иммунологические факторы; в 7–9 недель наибольшее значение имеют гормональные нарушения, в том числе и наличие антител к гормонам; в 10–16 недель основными этиологическими факторами являются аутоиммунные нарушения (АФС) и тромбофилии; а при сроках беременности более 16 недель основные причины репродуктивных потерь инфекции, истмикоцервикальная недостаточность, тромбофилии.
По данным литературы [8] у 88% женщин, с наличием репродуктивных потерь в анамнезе, выявляются те или иные значимые структурные изменения в репродуктивной системе. Этот факт дает основание проводить стандартное обследование всем пациенткам с наличием синдрома потери плода, включающее: бактериологическое исследование отделяемого из влагалища и полости матки, ПЦР-диагностику инфекций, передаваемых половым путем, исследование гормонального фона, системы гемостаза с определением наличия полиморфизма генов, определение иммунореактивности, УЗИ органов малого таза, медико-генетическое консультирование с определением кариотипа родителей.
Начало третьего тысячелетия вновь актуализировало проблему НБ, так как частота данной патологии стала увеличиваться практически во всех странах мира [8], широкое внедрение к практику новых диагностических и лечебных методов, основанных на достижениях современной науки, не улучшает ситуацию. Дискуссии на тему «Почему результаты антенатальной терапии меньше ожидаемых?» не могут определить основные детерминанты имеющегося неблагополучия, но ставят перед исследователями ряд перспективных, жизненно важных для человечества вопросов, без решения которых дальнейший прогресс перинатальной медицины невозможен.