Резидуальная ткань тимуса в переднем средостении что это
Резидуальная ткань тимуса в переднем средостении что это
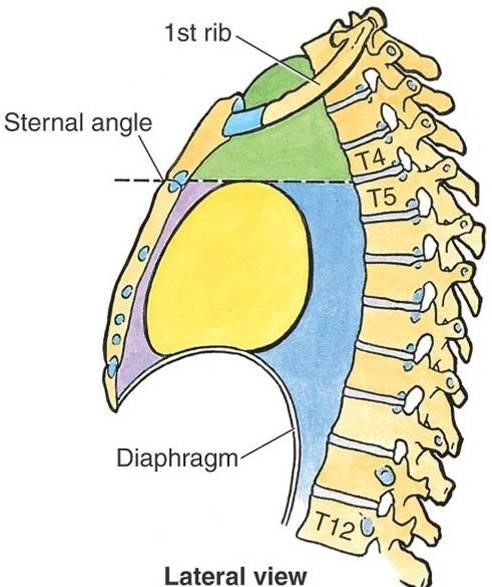
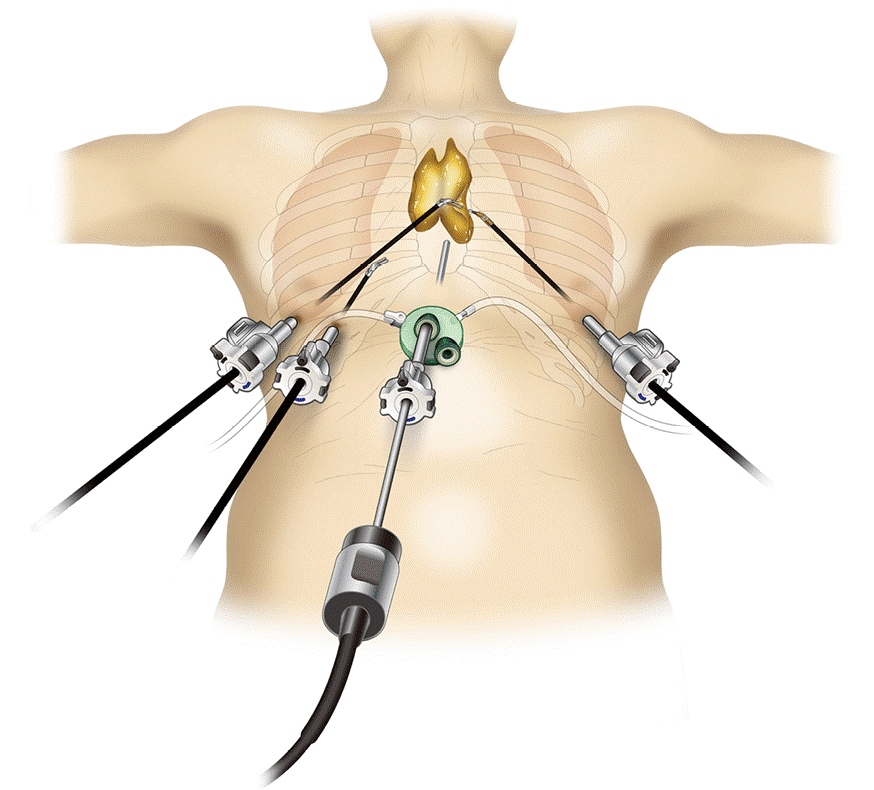
Тимус является одним из основных органов лимфатической системы, играющим ключевую роль как в клеточном, так и в гуморальном иммунитете. Данный орган развивается из вентральной части глоточного кармана, покрыт капсулой и состоит из двух долей, расположенных в непосредственной близости от верхнего края перикарда, проксимальных отделов восходящей аорты и легочного ствола. Однако ткань тимуса может выявляться в любом месте на протяжении от шеи до реберно-диафрагмального угла.
Тимус имеет форму пирамиды с широким основанием внизу и двумя узкими рогами вверху. Несмотря на то что тимус активно функционирует на протяжении всей жизни, с возрастом наблюдается его жировая инволюция. У взрослых тимус при рентгенографии в норме не визуализируется, однако у лиц моложе 40 лет его можно увидеть при КТ или МРТ. После 40 лет по причине завершения жировой инволюции ткань тимуса обнаруживают редко.
а) Опухоли тимуса. Согласно классификации Всемирной организации здравоохранения (ВОЗ) опухоли, развивающиеся в тимусе или в переднем средостении вблизи тимуса, делят на эпителиальные новообразования (тимома, карцинома тимуса и карциноид тимуса), герминативноклеточные новообразования, медиастинальную лимфому (может поражать тимус), мезенхимальные новообразования (тимолипома, липома, липосаркома), эктопические новообразования (происходят из щитовидной или паращитовидной железы) и метастазы. Гистологическая классификация тимом, разработанная ВОЗ, широко используется в патологической анатомии, но в клинической практике ее применение затруднено из-за расхождений между специалистами по интерпретации полученных результатов, гистологической гетерогенности данного типа опухолей и слабой корреляции с клиническим исходом.
Однако следует отметить, что во многих опубликованных статьях тимомы согласно гистологической классификации ВОЗ подразделяют на опухоли с низким риском (типы А, АВ и В1) и опухоли с высоким риском (типы В2 и ВЗ).
Новообразования тимуса встречаются редко и составляют менее 1 % от всех злокачественных опухолей у взрослых. Вследствие этого опухоли тимуса изучены плохо, и публикации на эту тему, как правило, ограничиваются одноцентровыми ретроспективными обзорами, охватывающими большой промежуток времени. В 2010 году для «обеспечения строгих требований к структуре, организации и научности» исследований, посвященных злокачественным опухолям тимуса и средостения, была организована Международная группа по изучению злокачественных новообразований тимуса (ITMIG).
ITMIG представляет собой мультидисциплинарную группу экспертов (в том числе врачей лучевой диагностики), признанную Международным союзом по борьбе с раком (UICC) и Американским объединенным комитетом по изучению рака (AJCC).
Для стадирования множества злокачественных новообразований были разработаны классификации TNM, учитывающие распространенность первичной опухоли (Т), наличие метастазов в регионарных лимфатических узлах (N) и отдаленных метастазов (М). Однако стадирование эпителиальных опухолей тимуса обычно проводится согласно классификации Масаока-Кога. В настоящее время ITMIG работает над тем, чтобы создать в сотрудничестве с Международной ассоциацией по изучению рака легких (IASLC) классификацию TNM для стадирования злокачественных опухолей тимуса. Рассматривается возможность включения такой классификации в 8-е издание системы TNM, разрабатываемой AJCC/UICC.
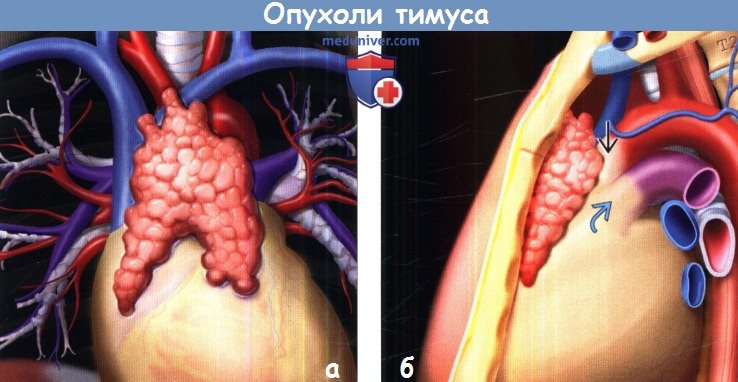
(б) На рисунке изображено положение тимуса в норме. Тимус локализуется в преваскулярном средостении и прилежит к начальным отделам легочного ствола и восходящей аорты.
б) Лучевая диагностика опухолей тимуса. Новообразования тимуса могут быть выявлены случайно вследствие обнаружения патологических изменений при отсутствии соответствующих симптомов, к которым относят паратимический синдром, связанный с неоплазией тимуса (например, при миастении, множественной эндокринной неоплазии), и симптомы, обусловленные объемным воздействием опухоли или ее местнодеструирующим ростом. Знание нормальной лучевой анатомии средостения и тимуса имеет большое значение для дифференцирования опухолевых образований тимуса с неопухолевыми. Диффузное увеличение тимуса может наблюдаться при его гиперплазии или лимфоматозном поражении. Изолированное объемное образование с большей вероятностью соответствует первичной злокачественной опухоли тимуса, часто — эпителиальной.
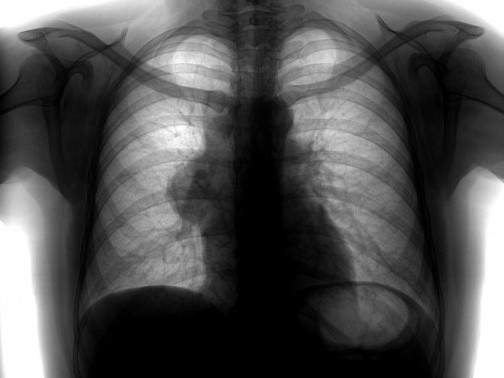
1. Рентгенография. Рентгенография органов грудной клетки является первичным методом диагностики, при котором можно выявить патологические изменения в тимусе. Заподозрить наличие патологического образования можно по изменению медиастинальных линий и полос, в том числе по утолщению передней соединительной линии, и по изменению контуров средостения, однако изменения могут быть выражены слабо. Вследствие внелегочной локализации патологические образования тимуса могут характеризоваться наличием симптома неполного контура и не визуализироваться при исследовании во взаимно перпендикулярных проекциях. Кроме того, небольшие патологические образования, расположенные по срединной линии, в прямой проекции могут не выходить за контур средостения.
При распространенных опухолях и опухолях с местнодеструирующим ростом могут обнаруживаться неровный их контур, высокое стояние купола диафрагмы вследствие инвазии диафрагмального нерва и «падающие» метастазы в плевре.
2. КТ. КТ с контрастным усилением является методом выбора для диагностики опухолей тимуса.
Такие опухоли обычно возникают у взрослых лиц, у которых тимус подвергается жировой инволюции. Поэтому мягкотканные опухоли тимуса хорошо визуализируются на фоне жировой ткани. Использование контрастного вещества позволяет выявлять признаки инвазивного роста новообразований: инфильтрацию жировой клетчатки средостения, исчезновение кпетчаточных пространств между патологическим образованием и прилежащими структурами, циркулярный охват или инвазию легких или сердца и сосудов, лимфаденопатию, сопутствующий плевральный или перикардиальный выпот и мягкотканные узелки и объемные образования.
КТ позволяет осуществлять предоперационное стадирование эпителиальных опухолей тимуса (особенно тимомы) и определять тактику лечения пациентов: выполнять хирургическое вмешательство, проводить неоадъювантную терапию при местно-распространенных опухолях или паллиативную химиотерапию при наличии лимфогенных и гематогенных метастазов. Крометого, КТ предпочтительнее использовать для оценки состояния пациентов со злокачественным новообразованием тимуса после проведенного лечения.
3. МРТ. МРТ также используется для выявления патологических изменений в тимусе и позволяет дифференцировать гиперплазию с неоплазией, поскольку первая характеризуется выраженным снижением интенсивности сигнала в противофазе. Кроме того, с помощью МРТ можно дифференцировать кистозные образования тимуса: в стенках кистозных опухолей в отличие от кист могут выявляться узелки. Также МРТ можно применять у тех пациентов, кому противопоказано вводить йодсодержащее контрастное вещество, что позволяет оценивать сосуды на предмет наличия инвазии даже без проведения контрастного усиления.
4. ФДГ-ПЭТ/КТ. ФДГ-ПЭТ/КТ не позволяет с точностью дифференцировать гиперплазию тимуса и неоплазию или так называемые тимомы с низким риском и тимомы с высоким риском. Однако данный метод используется для оценки злокачественных опухолей тимуса (например, карциномы) и обнаружения отдаленных метастазов и метастазов в лимфатических узлах.
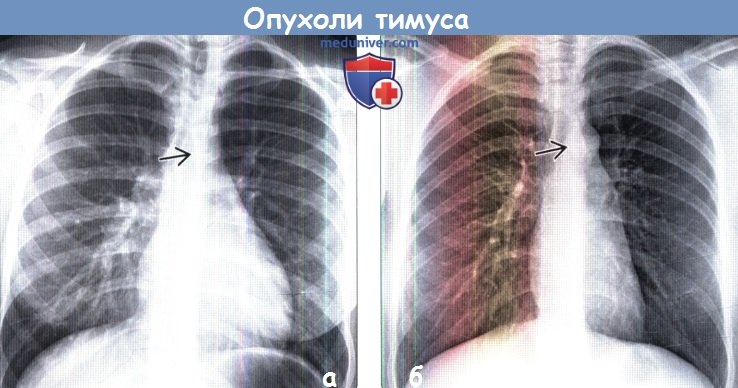
(б) Женщина 27 лет с диффузным токсическим зобом. При рентгенографии органов грудной клетки в ПП проекции визуализируется незначительное утолщение передней соединительной линии вследствие увеличения тимуса, вызванного его гиперплазией. При рентгенографии объемные образования тимуса могут проявляться слабо выраженными патологическими изменениями. 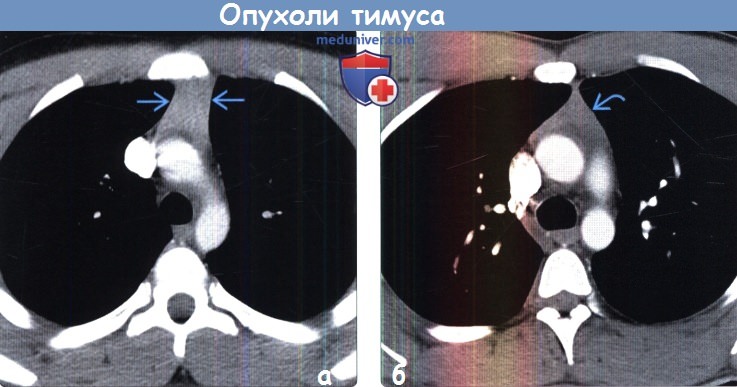
(б) У мужчины 21 года при КТ с контрастным усилением в преваскулярном отделе средостения визуализируется нормальный тимус, характеризующийся треугольной формой, гомогенной структурой и мягкотканной плотностью. Это нормальная лучевая картина для данного возраста.
Редактор: Искандер Милевски. Дата публикации: 6.2.2019
Опухоли средостения: что это такое, классификация.
Опухоли средостения – общее название новообразований, которые расположены в медиастинальном пространстве груди. В 40% случаев диагностирования опухоли являются злокачественными, и тогда ставится диагноз рак средостения. Все опухоли делятся на две большие группы – первичные и вторичные. В первом случае речь идет о тех новообразованиях, которые формируются непосредственно в области средостения, во втором – опухоли образуются сначала в тканях, расположенных вне обозначенной области, а рак средостения развивается уже из метастаз. Иногда опухоли средостения называют рак тимуса, но это не совсем корректное обозначение диагноза. Дело в том, что он обозначает наличие злокачественных клеток в вилочковой железе, тогда как опухоли средостения могут начать свой рост и из других структур.
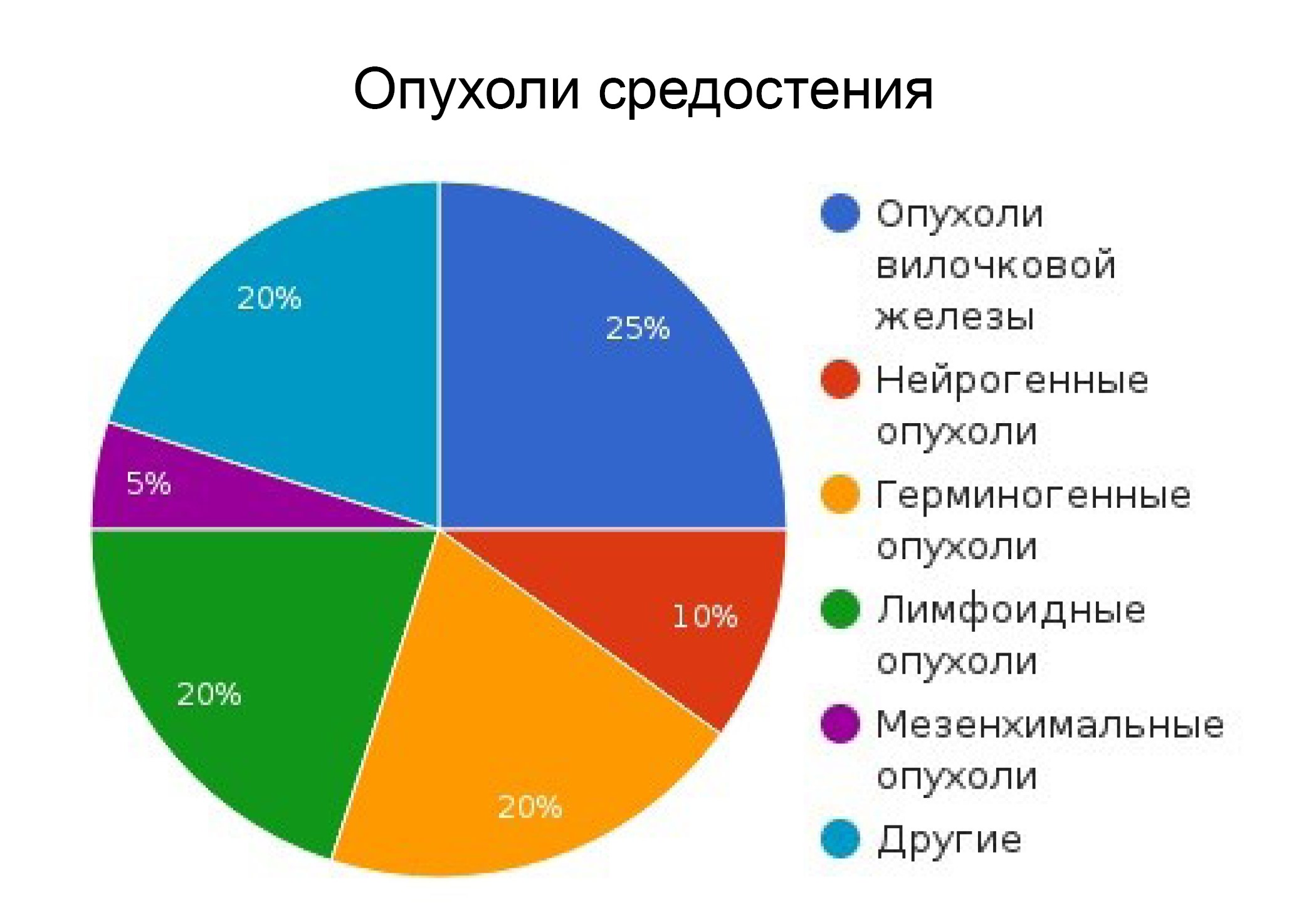
В зависимости от локализации опухоли различают следующие виды злокачественных новообразований:
Злокачественные новообразования средостения диагностируются чаще всего в возрасте 18-45 лет, какой-то гендерной предрасположенности не отмечается.
Отдельно в медицине рассматриваются мезенхимальные опухоли – представляют собой рак мягких тканей, к таковым относятся липомы и гемангиомы, лейомиосаркомы и фибромы. Поражают разные части средостения, относятся к группе вторичных, потому что «вырастают» из метастаз.
К редким опухолям средостения относятся липо- и фибросаркомы. Их опасность заключается в том, что они долгое время протекают бессимптомно и пациент обращается за помощью к врачу при выраженных нарушениях, когда рак находится уже на 3 и 4 стадии развития. Также к этой группе относится рак тимуса (тимома) – развивается в клетках вилочковой железы.
Какие симптомы укажут на рак средостения?
Рак может протекать в двух стадиях – бессимптомной и с выраженными признаками. Продолжительность прогрессирования опухоли средостения без симптомов зависит от нескольких факторов – место локализации новообразования, уровень общего иммунитета, возраст человека. Часто бессимптомно протекающий рак диагностируется случайно, во время проведения стандартной процедуры флюорографии в рамках диспансеризации.
К основным признакам рака средостения относятся:
Злокачественные опухоли растут достаточно быстро, поэтому переход из бессимптомной стадии в форму с выраженной клинической картиной недолгий. Могут проявляться и дополнительные симптомы типа отечности верхней части туловища и лица, синюшного цвета лица, расширения подкожных вен шеи.
Самым ранним проявлением рака средостения считается болевой синдром, особенно часто он проявляется при раке тимуса. В таком случае боли идентичны приступам стенокардии. Существует и ряд специфичных признаков опухолей средостения:
Общие симптомы, слабовыраженная клиническая картина, многообразие признаков, которые присущи и другим патологиям, делают диагностику только по жалобам пациента и стандартным обследованиям практически невозможной. Кроме этого, опухоли средостения могут быть и доброкачественными – например, рак тимуса по своей клинической картине полностью идентичен признакам доброкачественных новообразований в вилочковой железе.
Диагностика опухоли средостения.
Опухоль средостения может быть диагностирован инструментальными методами, которые являются самыми информативными:
Если перечисленных обследований недостаточно, то назначается хирургическая биопсия. Морфологическое исследование биологического материала позволяет полностью охарактеризовать рак средостения. Эта манипуляция важна для классификации опухоли – будет ли диагностирован именно рак тимуса или опухоль представляет собой доброкачественное образование.
Если есть подозрение на тимому (рак тимуса), то целесообразно проводить ультразвуковое исследование. Оно не выявит опухоль средостения, но даст возможность оценить состояние лимфатических узлов и жировой ткани в подключичной области.
К общим методам диагностики относятся анализы крови (общий, биохимический, коагулограмма), анализ мочи (общий), ЭКГ.
Лечение опухолей средостения.
Самым эффективным методом лечения опухолей средостения считается его хирургическое удаление, которое всегда сопровождается и специфической терапией. Если диагноз был поставлен на ранней стадии, врач может четко определить размер и форму опухоли, то применяется радиохирургический метод ее удаления по системе КиберНож. В случае больших размеров опухоли средостения удаляются классическим хирургическим методом с последующей химиотерапией. Диагностирование рака на поздней стадии делает нецелесообразным оперативное удаление новообразования, поэтому пациенту назначают только поддерживающее лечение (химиотерапия или лучевая) – рак средостения прекращает стремительно разрастаться, снижается вероятность распространения метастаз, облегчается симптоматика.
Если диагностирован рак тимуса (тимома), то врач опирается на данные исследований – каков размер опухоли средостения, есть ли ее разрастание. В некоторых случаях сначала проводится несколько курсов химиотерапии и только после этого назначается хирургическое лечение. Дополнительно, после проведения операции по удалению опухоли средостения, пациенту назначают гормональные препараты, иммуноподдерживающие средства.
Принимать решение о проведении терапевтического лечения или хирургического удаления опухоли средостения может только лечащий врач. Операция выполняется только в том случае, если специалист будет уверен в том, что он сможет удалить сразу все новообразование. Так как диагноз рак средостения часто ставится на поздних стадиях заболевания, то даже хирургические методы могут быть бесполезными по причине распространения метастаз, поражения внутренних органов и мягких тканей вокруг средостения.
Прогноз рака средостения.
Теоретически прогнозы на выздоровление при диагностировании опухоли средостения (рака тимуса) положительные. Но проблема заключается в сложностях диагностики – клиническая картина не типичная для злокачественных образований, часто люди либо предпринимают попытки лечения сами, либо обращаются со стандартными жалобами к врачу и им ставят неверный диагноз. Пока проводится лечение неверного заболевания, время проходит и наступает рак, средостения достигает тяжелой стадии. При своевременном выявлении рака тимуса вероятность благоприятного исхода составляет 68%.
Опухоли средостения (рак тимуса) возможно вылечить, но при условии своевременного выявления. Хирургический метод и последующая химиотерапия дают возможность полностью выздороветь. По причине неспецифической клинической картины диагностирование на ранней стадии затруднено, поэтому важно проходит диспансеризацию – это реальный шанс полностью избавиться от злокачественных образований.
Филиалы и отделения, в которых лечат опухоль средостения (рак тимуса)
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
В Отделе торакоабдоминальной онкохирургии
Заведующий отделом – д.м.н. А.Б. РЯБОВ
В Отделении торакальной хирургии
Контакты: (495) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Заведующий Отделом торакоабдоминальной онкологии – д.м.н. В.Ю. СКОРОПАД
Опухоли средостения
Опухоли средостения, или по-другому медиастинальные опухоли — это новообразования, которые берут свое начало из органов средостения. Средостение – это область, ограниченная легкими по бокам, грудиной спереди и позвоночником сзади. К органам средостения относятся сердце, аорта, пищевод, тимус, трахея, лимфатические узлы, сосуды и нервы.
Кто находится в «зоне риска»?
Медиастинальные опухоли встречаются достаточно редко. Они могут развиваться в любом возрасте и из любых органов и тканей, которые находятся в средостении, однако в большинстве случаев их диагностируют у пациентов от 30 до 50 лет. В детском возрасте чаще встречаются опухоли заднего средостения. Они обычно происходят из нервной ткани и, в большинстве случаев, не злокачественные. У взрослого населения преобладают опухоли переднего средостения – обычно там располагаются лимфомы и тимомы.
Классификация образований средостения
Средостение анатомически делится на 3 зоны. Соответственно этим зонам классифицируются и опухоли средостения.
Клиническая картина
Чаще всего опухоли средостения являются случайной находкой при рентгенологических исследованиях, так как до 40% опухолей клинически не проявляются. Клинические проявления опухоли средостения будут зависеть от следующих факторов:
В зависимости от вышеописанных факторов клиническая картина может быть различной. Самые частые симптомы можно разделить на две группы:
Диагностика
Рентгенологический метод является основным для визуализации новообразования средостения. Компьютерная томография позволяет оценить локализацию опухоли и спланировать дальнейшее обследование.
Без гистологической верификации поставить окончательный диагноз невозможно. При вовлечении в процесс пищевода или трахеи выполняют эндоскопическое исследование для взятия биопсии и визуализации изменений.
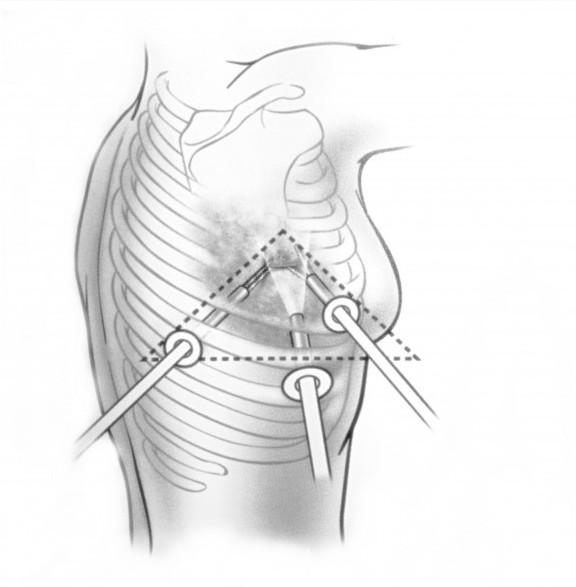
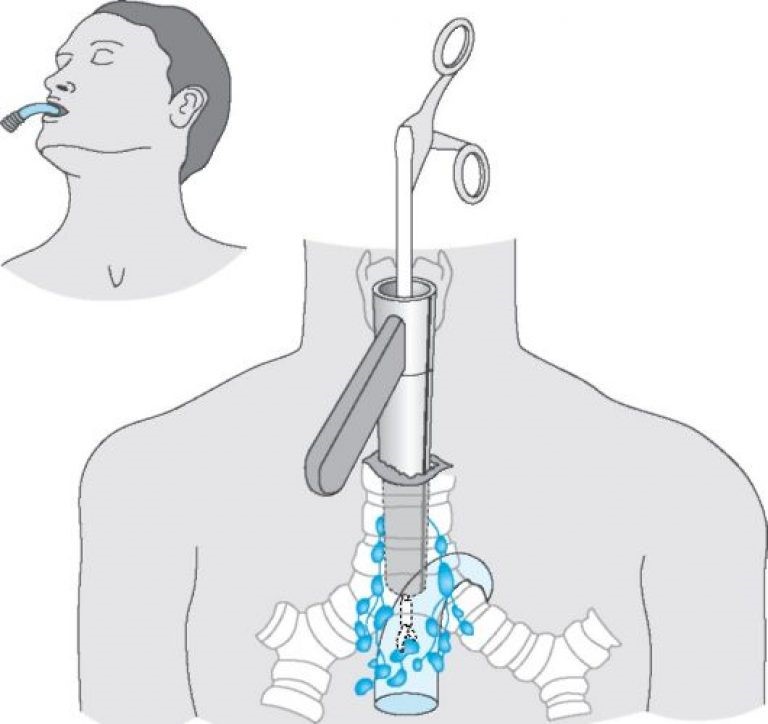
При невозможности получить образец ткани для исследования эндоскопически применяются инвазивные методы: трансторакальная биопсия, медиастиноскопия, видеоторакосокпия. Последние два метода — это серьезные операции, которые проводятся в специализированных медицинских учреждениях.
Лечение
В связи с разнообразием возможных причин медиастинальные опухоли лечатся в зависимости от типа опухоли:
Профилактика и прогнозы
К сожалению, достоверных методов профилактики для опухолей средостения не выявлено. Но результаты можно существенно улучшить, если выявить заболевание на ранней стадии. Если симптомы, описанные ранее не проходят в течение двух недель, возможно стоит обратиться за квалифицированной медицинской помощью. Прогнозы в данном случае трудно давать, они зависят, типа опухоли и ее злокачественности от проводимого лечения.
Список литературы:
1) Клинические рекомендации Ассоциации онкологов России (АОР, 2020)
2) Барболина Т. Д., Бычков М. Б., Аллахвердиев А. К., Борисова Т. Н., Владимирова Л. Ю., Герасимов С. С., Деньгина Н. В., Козлов Н. А., Лактионов К. К., Левченко Е. В., Малютина Д. В., Пикин О. В. Практические рекомендации по лекарственному лечению опухолей вилочковой железы (тимомы и рака тимуса). Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2020 (том 10). С. 608-619.
3) Руководство по химиотерапии опухолевых заболеваний/ под ред. Н.И. Переводчиковой, В.А. Горбуновой. – 4-е изд., расширенное и дополненное. – М.: Практическая медицина, 2018.-688с.
4) Рациональная фармакотерапия в онкологии: руководство для практикующих врачей/под.ред. М.И. Давыдова, В.А. Горбуновой. – М.: Литтерра, 2017. – 880с. (Серия «Рациональная фармакотерапия»).
5) Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. Злокачественные новообразования в России в 2018 году. (заболеваемость и смертность) — М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, — 2019. –илл.-250с.
6) Пикин О.В. et al. Опухоли средостения: сборник под ред. академика РАН, профессора А.Д. Каприна. М.: Молодая гвардия, 2019. 232 p.
Тимома
Тимома – гетерогенная группа новообразований, различных по гистогенезу и степени зрелости, берущих начало из эпителиальной ткани вилочковой железы. Варианты клинического течения тимомы могут быть различны: от бессимптомного до выраженного (компрессионный, болевой, миастенический, интоксикационный синдром). Топографо-анатомический и этиологический диагноз устанавливается с помощью лучевых методов (рентгенография, КТ средостения), трансторакальной пункции, медиастиноскопии, исследования биоптата. Лечение хирургическое: удаление тимомы вместе с вилочковой железой и жировой клетчаткой переднего средостения, дополненное по показаниям химиолучевой терапией.
Общие сведения
Тимома – органоспецифическая опухоль средостения, происходящая из клеточных элементов мозгового и коркового вещества тимуса. Термин «тимома» был введен в употребление в 1900 году исследователями Grandhomme и Scminke для обозначения различных опухолей вилочковой железы. Тимомы составляют 10-20% всех новообразований медиастинального пространства. В 65-70% случаев тимомы имеют доброкачественное течение; инвазивный рост с прорастанием плевры и перикарда отмечается у 30% пациентов, отдаленное метастазирование – у 5%. Несколько чаще тимомы развиваются у женщин, болеют преимущественно лица 40-60 лет. На детский возраст приходится менее 8% опухолей тимуса.
Причины формирования опухолей вилочковой железы неизвестны. Предполагается, что тимомы могут иметь эмбриональное происхождение, быть связаны с нарушением синтеза тимопоэтина или иммунного гомеостаза. Факторами, провоцирующими рост и развитие опухоли, могут служить инфекционные заболевания, радиационное воздействие, травмы средостения. Замечено, что тимомы часто сочетаются с различными эндокринными и аутоиммунными синдромами (миастенией, дерматомиозитом, СКВ, диффузным токсическим зобом, синдромом Иценко-Кушинга и др.).
Строение и функции вилочковой железы
Вилочковая железа, или тимус располагается в нижней части шеи и переднем отделе верхнего средостения. Орган образован двумя асимметричными долями – правой и левой. В свою очередь, каждая доля представлена множеством долек, состоящих из коркового и мозгового вещества и заключенных в соединительнотканную строму. В вилочковой железе различают два типа ткани – эпителиальную и лимфоидную. Эпителиальные клетки секретируют тимические гормоны (тимулин, a-, b-тимозины, тимопоэтины и пр.), лимфоидная ткань состоит из Т-лимфоцитов различной степени зрелости и функциональной активности.
Таким образом, вилочковая железа одновременно является железой внутренней секреции и органом иммунитета, обеспечивающим взаимодействие эндокринной и иммунной систем. После 20 лет тимус подвергается возрастной инволюции; после 50 лет паренхима тимуса на 90% замещается жировой и соединительной тканью, сохраняясь в виде отдельных островков, лежащих в клетчатке средостения.
Классификация тимом
В онкологии различают три типа тимом: доброкачественную, злокачественную тимому 1-го типа (с признаками атипии, но относительно доброкачественным течением) и злокачественную тимому 2-го типа (с инвазивным ростом).
В зависимости от удельного веса лимфоидного компонента в тимоме дифференцируют лимфоидные (более 2/3 всех клеток опухоли представлено Т-лимфоцитами), лимфоэпителиальные (Т-лимфоциты составляют от 2/3 до 1/3 клеток) и эпителиальные тимомы (Т-лимфоцитами представлено менее 1/3 всех клеток).
Основываясь на степени инвазивного роста, выделяют 4 стадии тимомы:
Симптомы тимомы
Клинические проявления и течение тимомы зависит от ее типа, гормональной активности, размеров. Более чем в половине случаев опухоль развивается латентно и обнаруживается во время профилактического рентгенологического исследования.
Инвазивные тимомы вызывают компрессионный медиастинальный синдром, который сопровождается болями за грудиной, сухим кашлем, одышкой. Сдавление трахеи и крупных бронхов проявляется стридором, цианозом, дыхательной недостаточностью. При синдроме компрессии верхней полой вены возникает одутловатость лица, синюшность верхней половины туловища, набухание шейных вен. Давление растущей опухоли на нервные узлы обусловливает развитие синдрома Горнера, осиплость голоса, элевацию купола диафрагмы. Сдавливание пищевода сопровождается расстройством глотания – дисфагией.
По различным данным, от 10 до 40% тимом сочетаются с миастеническим синдромом. Больные отмечают снижение мышечной силы, быструю утомляемость, слабость мимических мышц, двоение в глазах, поперхивание, нарушения голоса. В тяжелых случаях может развиться миастенический криз, требующий перехода к ИВЛ и зондовому питанию.
В поздних стадиях злокачественной тимомы появляются признаки раковой интоксикации: лихорадка, анорексия, снижение массы тела. Нередко тимоме сопутствуют различные гематологические и иммунодефицитные синдромы: апластическая анемия, тромбоцитопеническая пурпура, гипогаммаглобулинемия.
Диагностика
Диагностика тимомы проводится торакальными хирургами с привлечением онкологов, рентгенологов, эндокринологов, неврологов. При клиническом осмотре может выявляться расширение вен грудной клетки, выбухание грудины в проекции опухоли; увеличение шейных, надключичных, подключичных лимфоузлов; признаки компрессионного синдрома и миастении. Физикальное исследование обнаруживает расширение границ средостения, тахикардию, свистящие хрипы.
На рентгенограмме грудной клетки тимома имеет вид объемного образования неправильной формы, расположенного в переднем средостении. КТ грудной клетки значительно расширяет объем информации, полученный при первичной рентгендиагностике и в ряде случаев позволяет поставить морфологический диагноз. Уточнение локализации и взаимоотношения новообразования с соседними органами при КТ средостения позволяет в дальнейшем выполнить трансторакальную пункцию опухоли средостения, что чрезвычайно важно для гистологического подтверждения диагноза и верификации гистологического типа тимомы.
Для визуального исследования средостения и выполнения прямой биопсии проводится диагностическая медиастиноскопия, парастернальная торакотомия или торакоскопия. Диагноз миастении уточняется с помощью электромиографии с введением антихолинэстеразных препаратов. Дифференциально-диагностические мероприятия позволяют исключить другие объемные процессы в средостении: загрудинный зоб, дермоидные кисты и тератомы средостения.
Лечение тимом
Лечение опухолей вилочковой железы проводится в отделениях торакальной хирургии и онкологии. Хирургический метод является основным в лечении тимомы, поскольку только тимэктомия обеспечивает удовлетворительные отдаленные результаты. При доброкачественных тимомах оперативное вмешательство заключается в удалении опухоли вместе с вилочковой железой (тимомтимэктомия), жировой клетчаткой и лимфатическими узлами средостения. Такой объем резекции диктуется высоким риском рецидива опухоли и миастении. Операция выполняется из срединного стернотомического доступа.
При злокачественных новообразованиях тимуса операция может дополняться резекцией легкого, перикарда, магистральных сосудов, диафрагмального нерва. Послеоперационная лучевая терапия показана при II и III стадиях тимомы. Кроме этого, облучение является ведущим методом лечения неоперабельных злокачественных тимом IV стадии. В настоящее время большее значение в лечении инвазивных тимом получает трехэтапное лечение, включающее неоадъювантную химиотерапию, резекцию опухоли и лучевую терапию.
В послеоперационном периоде у больных, перенесших тимэктомию, может случиться миастенический криз, который требует проведения интенсивной терапии, трахеостомии, ИВЛ, длительного назначения антихолинэстеразных препаратов.
Отдаленные результаты лечения доброкачественных тимом хорошие. После удаления опухоли исчезают или значительно уменьшаются симптомы миастении. У больных злокачественной тимомой, прооперированных на ранних стадиях, 5-летняя выживаемость достигает 90%, на III стадии – 60-70%. Неоперабельные формы онкологического заболевания имеют плохой прогноз с летальностью 90% в течение ближайших 5 лет.