Резектабельная опухоль что это
Резектабельная опухоль что это
© С.В. Горчаков, И.В. Правосудов, С.В. Васильев, В.В. Олейник, М.В. Оношко, Д.Е. Попов, 2015
1 фГОУ ВПО «Санкт-Петербургский государственный университет», г. Санкт-Петербург
2 СПб ГБУЗ «Городская многопрофильная больница № 2», г. Санкт-Петербург
3 ФГОУ ВПО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова», г. Санкт-Петербург
Горчаков Сергей Васильевич — врач-хирург хирургического отделения ГМПБ №2, ассистент кафедры госпитальной хирургии СПб ГУ, тел. +7-905-205-67-86, e-mail: Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Реферат. На основании литературных данных выполнен анализ современных подходов к лечению колоректального рака (КРР) с метастазами в печень. В течение последних 10–15 лет значительно изменилось отношение к пациентам с диссеминированными формами КРР благодаря прогрессу в хирургическом лечении метастатических поражений печени и появлению новых лекарственных препаратов. Тенденция к расширению показаний к удалению резектабельных метастазов в печени при резектабельной первичной опухоли поддерживается большинством специалистов. Показано, что использование неоадъювантной лучевой и химиолучевой терапии позволило снизить частоту местных рецидивов, увеличить частоту лечебного патоморфоза и уменьшить частоту отдаленного метастазирования. Использование неоадъювантной лучевой терапии вместе с современными схемами ХТ (FOLFOX, XELOX) рассматривается в отношении лечения прогностически «благоприятных» групп диссеминированных больных, которым можно выполнить операции в «радикальном» объеме и увеличить частоту сфинктеросохранных операций, улучшая качество жизни. Наиболее перспективным направлением в лечении синхронных внутрипеченочных метастазов является выполнение хирургических вмешательств, при которых одновременно осуществляется удаление первичной опухоли и метастазов в печени. Сделан вывод о необходимости дальнейших исследований для повышения клинической эффективности и безопасности лечения пациентов КРР с изолированными метастазами в печени.
Ключевые слова: колоректальный рак, метастазы, печень, резекция, химиотерапия, адъювантная терапия.
Введение
Ежегодно от рака толстой кишки умирает около 50 000 человек [1]. В 2009 г. в России зарегистрировано 32 334 новых случая рака ободочной кишки и 25 029 новых случаев рака прямой кишки (РПК) [2, 3]. В общей сложности 20% пациентов с колоректальным раком (КРР) на момент постановки диагноза имеют отдаленные метастазы, а примерно у 25-30% из них обнаруживаются изолированные метастазы в печени. Метастазирование в печень происходит по системе воротной вены, обеспечивающей перенос опухолевых эмболов прямым путем в капиллярную сеть печени, которая при данном типе метастазирования служит первым фильтром. Средняя продолжительность жизни больных с метастатическим поражением печени без специфического лечения составляет менее 1 года, а при синхронном метастазировании — 4,5 месяца с момента установления диагноза [4, 5]. Прогноз в отношении больных с метастатическим колоректальным раком значительно улучшился за последние 10-15 лет в связи с появлением эффективных схем химиотерапии, позволяющих перевести значительное количество пациентов в кандидаты для хирургического вмешательства [5]. Тем не менее, лечение больных КРР с метастатическим поражением печени остается сложной задачей и, по мнению большинства специалистов, должно быть комбинированным, включающим хирургический метод, химиотерапию (ХТ), иммунотерапию. Метод лечения выбирается в зависимости от общего состояния больного, клинического течения, гистологической характеристики, размеров, анатомической локализации первичной опухоли и отдаленных метастазов, взаимосвязи с соседними органами, количества опухолевых узлов в паренхиме печени, а также количества пораженных метастазами органов.
Цель работы — анализ современных подходов к лечению колоректального рака с метастазами в печень. Если в конце прошлого века хирургические вмешательства носили симптоматическую направленность и, как правило, сопровождались (до 80%) формированием разгрузочных колостом или обходных межкишечных анастомозов 5, то в течение последних 10-15 лет значительно изменилось отношение к пациентам с диссеминированными формами КРР. Это стало возможным благодаря как прогрессу в хирургическом лечении метастатических поражений печени, так и появлению новых лекарственных препаратов. Несмотря на то, что на сегодняшний день остается много нерешенных вопросов в выборе варианта, объема и сроках вмешательства, признано целесообразным выполнение резекций печени по поводу метастазов КРР. Тенденция к расширению показаний к удалению резектабельных метастазов в печени при резектабельной первичной опухоли поддерживается большинством специалистов [6]. Было показано, что выполнение оперативных вмешательств как на первичном очаге, так и на отдаленных метастазах в программе комбинированного лечения только при условии R0-резекций не только увеличивает продолжительность жизни, но и позволяет достичь 5-летней выживаемости 7. Использование неоадъювантной лучевой и химиолучевой терапии позволило снизить частоту местных рецидивов практически до минимума (1-5%), увеличить частоту лечебного патоморфоза и снизить частоту отдаленного метастазирования [7]. Использование неоадъювантной лучевой терапии вместе с современными схемами ХТ (FOLFOX, XELOX) рассматривается в отношении лечения прогностически «благоприятных» групп диссеминированных больных (например, при наличии солитарных метастазов), которым можно выполнить операции в «радикальном» объеме и увеличить частоту сфинктеросохранных операций, улучшая качество жизни. При наличии синхронных внутрипеченочных метастазов многие специалисты склоняются к одновременному удалению первичной опухоли и метастазов в печени [5, 7, 8]. Общая 5-летняя выживаемость после хирургического удаления метастазов в печень достигает 35-58% [8]. Пациенты с нелечеными метастазами КРР имеют медиану выживаемости примерно 12 месяцев [9]. Учитывая, что хирургическая резекция остается лучшим методом лечения, были пересмотрены критерии резектабельности у больных с колоректальными метастазами с использованием вспомогательных подходов.
Критерии резектабельности метастазов печени при колоректальном раке
Еще в 1986 г. Ekberg H. et al. предложили несколько общих противопоказаний к резекции печени при метастазах КРР: 4 или больше очагов, наличие внепеченочного распространения, большой размер (более 5 см) метастазов и невозможность достигнуть негативного края резекции в 1 см. Впоследствии эти положения были подвергнуты критике с клинических и методологических позиций. Совершенствование системной химиотерапии и развитие дополнительных методов лечения, таких как радиочастотная абляция, существенно изменили подходы к лечению этих пациентов. В настоящее время химиотерапия позволяет перевести нерезектабельные метастазы в печени в резектабельные, в связи с чем прежние «правила резектабельности» были пересмотрены. В результате этого процент резектабельных опухолей вырос с 10-15% до 20-30%, а общая 5- и 10-летняя выживаемость примерно составили 33 и 23% соответственно [10]. Резекция печени стала методом выбора при лечении пациентов с метастазом КРР в печени при наличии возможности ее выполнения. У пациентов, не подвергнутых хирургическому вмешательству, пятилетняя выживаемость составляет менее 10% [11]. В некоторых работах сообщалось, что важную роль в прогнозе заболевания играют размеры метастазов [12]. Другие авторы [13] не смогли продемонстрировать эту связь, обосновывая мнение, что размеры метастазов в печени не могут быть приняты в качестве критерия для отказа от оперативного лечения. Одним из наиболее важных факторов, определяющих общую выживаемость после резекции печени по поводу изолированного метастаза КРР, является так называемый отрицательный хирургический край (R0-резекция) [14, 15]. Хирургическое вмешательство не показано, когда хирург считает достижение данного уровня резекции невозможным. В таких случаях должна рассматриваться возможность проведения химиотерапии, целью которой является достижение клинического регресса с дальнейшим рассмотрением вопроса о возможности и целесообразности хирургического лечения. Требует дальнейшего изучения и ряд других факторов, в частности, какой объем печени должен остаться после резекции (планируемый остаток печени), его функциональное состояние. Если пациент подвергся интенсивной ХТ, или у него имеется сопутствующее заболевание печени, следует оценивать гистопатологию «планируемого остатка печени». Резекцию следует выполнять лишь при том условии, если после операции сохранится по крайней мере 25-30% функциональной паренхимы печени, а при наличии сопутствующего заболевания печени или предшествующей ХТ объем остаточной функциональной паренхимы должен составить 30-40% [9]. Кроме того, должны быть сохранены по меньшей мере два непораженных сегмента печени, в которых сохранился нормальный сосудистый приток и отток, а также желчный дренаж. В качестве основных факторов риска послеоперационной печеночной недостаточности рассматриваются возраст старше 70 лет, цирроз, фиброз, гепатит, стеатоз, предоперационная химиотерапия, обструктивный холестаз и внутриоперационная кровопотеря или ишемия [16]. Согласно современным публикациям прогностическое значение клинико-патологических факторов определения «резектабельности» является непоследовательным и противоречивым. Исследования последних лет значительно изменили подход к его оценке, в настоящее время резектабельность определяется по 4 основным критериям:
1. Опухоль должна быть полностью резецирована. Резекции R0 как внутри-, так и внепеченочных метастазов должны быть выполнены.
2. Возможность оставить, по меньшей мере, два смежных сегмента печени.
3. Возможность сохранения сосудов и желчного дренажа от оставшихся сегментов.
4. Объем печени, оставшейся после резекции, должен быть адекватным, обычно не менее 20% от общего объема печени для нормальной паренхимы, 30–60% — при поражении печени в результате химиотерапии, стеатоза, или гепатита, или 40–70% — при наличии цирроза печени, в зависимости от степени дисфункции печени [17].
Увеличению количества больных КРР с резектабельными метастазами в печень способствовали возможности комбинации резекции с местным воздействием на опухолевые очаги, а также уменьшением остаточной доли печени. У части пациентов с множественными метастазами КРР выполняют резекцию правой доли и 4-го сегмента печени, при этом удаляется около 84% объема печени при отсутствии компенсаторной гипертрофии, вызываемой ростом опухоли [8]. Двухэтапная резекция печени может быть единственным лечебным подходом у пациентов с обширными билатеральными колоректальными метастазами в печень, которые не могут быть прооперированы одномоментно из-за недостаточного остаточного объема печени. Первоначальный опыт двухэтапной резекции печени без выполнения эмболизации воротной вены (PVE) был связан с высокой частотой развития печеночной недостаточности и высокой летальностью (9–15%). Позже появились данные о двухэтапной резекции печени, объединенной с PVE, свидетельствующие об отсутствии послеоперационной летальности [18]. Учитывая, что узлы в оставшемся объеме печени после PVE могут прогрессировать более быстро, метастазы в латеральных секторах обычно резецируются на первом этапе. Затем, если показано, выполняется PVE, и печень гипертрофируется в течение 3–4 недель [16]. В последние годы было продемонстрировано, что одновременная резекция печени столь же безопасна, как и пошаговая, при этом сокращается время пребывания пациента в стационаре [19, 20]. В то же время при больших объемах резекции печени при одновременном вмешательстве выявлен высокий уровень летальности [20], поэтому при обширных резекциях печени, например, при трисегментэктомии, следует прибегать к двухэтапным операциям.
Особенности проведения неоадъювантной химиотерапия при резектабельных метастазах в печени
До настоящего времени дискутируется вопрос о наличии преимуществ проведения предоперационной ХТ, назначаемой перед операцией по удалению резектабельных метастазов в печени. Исследование Европейской организации по исследованиям и лечению рака (EORTC) 40983 является на данный момент единственным рандомизированным исследованием III фазы, в котором было выполнено сравнение эффективности сочетания предоперационной ХТ и хирургического вмешательства с проведением только хирургического вмешательства. 364 пациента, у которых было не более четырех метастазов в печени, были случайным образом разделены на две группы, пациенты одной из которых подверглись исключительно оперативному лечению, а пациентам второй группы было назначено по шесть пре- и постоперационных курсов 5-фторурацила и оксалиплатина (FOLFOX4). Было установлено, что абсолютные значения выживаемости без прогрессирования увеличились на 9,2% в группе, получавшей химиотерапию (p=0,025). В общей сложности 84% всех больных завершили курс предоперационной химиотерапии, в то время как 76% пациентов, перенесших резекцию, прошли полный постоперационный курс. Предоперационная химиотерапия способствовала уменьшению размеров метастазов в печени у 30 и 43% пациентов, у которых проявился объективный ответ на лечение (у 3% полный ответ, у 40% — частичный), в то время как у 7% пациентов на фоне предоперационной химиотерапии опухоль продолжала прогрессировать. Частота осложнений была выше в группе, получавшей химиотерапию (25% против 16%, p=0.04), однако это не повлияло на уровень постоперационной смертности данной категории больных [12]. Согласно обновленным результатам этого исследования, выживаемость при среднем наблюдении в течение более 8,5 лет является практически одинаковой, при этом пятилетняя выживаемость составила 50% в обеих группах [14]. Следует отметить, что на сегодняшний день в доступной литературе отсутствуют сообщения об исследованиях по оценке эффективности таргетных лекарственных средств (ЛС) к VEGF или рецепторам EGFR при лечении больных с первоначально резектабельными метастазами в печени. Adam R. et al. (2010) провели ретроспективное обследование 1471 пациента с одиночными метахронными метастазами в печени, 169 из которых получили предоперационную ХТ, 1302 не получали такого лечения. Доля R0-резекций была приблизительно одинакова в обеих группах, показатель пятилетней выживаемости составил примерно 60% в обеих группах. Назначение предоперационной ХТ не повлияло на выживаемость, однако были выделены факторы, оказывающие негативное влияние на выживаемость, в частности, возраст старше 70 лет, поражение лимфоузлов первичной опухолью, срок от выявления опухоли до появления метастазов менее 12 месяцев, уровень РЭА более 5 нг/мл в момент постановки диагноза, диаметр опухоли более 5 см, отсутствие послеоперационной химиотерапии. Назначение послеоперационной химиотерапии существенно улучшило пятилетнюю выживаемость среди пациентов с метастазами в печени более 5 см в диаметре (58% против 33%, p Опубликовано в №4 2015
ХИРУРГИЧЕСКАЯ ТАКТИКА ПРИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЯХ ПЕЧЕНИ
Резектабельность злокачественных новообразований печени
Переносимость больным резекции печени
Решение о переносимости больным резекции печени принимается с учётом 2 позиций: оценки общего состояния пациента и оценки дооперационного функционального резерва печени.
При оценке общего состояния больного в предоперационном периоде особое внимание следует обращать на наличие сахарного диабета, хронических респираторных заболеваний, ишемической болезни сердца, сердечной недостаточности, так как помимо повышения общего риска оперативного вмешательства эти заболевания значительно снижают регенераторную активность печени, также как и пожилой и старческий возраст пациентов.
Функциональные резервные возможности печени оценивают на основании комплекса биохимических показателей крови, таких как уровень общего белка, альбумина, билирубина, аминотрансфераз, псевдохолинэстеразы, данных коагулограммы, а также показателей лидокаинового теста и результатов определения в сыворотке крови уровня протеина С (витамин К-зависимого антикоагулянта, синтезируемого печенью).
Проведённый анализ информативности основных параметров функционального резерва печени показал, что наиболее чувствительными лабораторными показателями, отражающими вероятность развития тяжёлой формы печёночной недостаточности, оказались дооперационные уровни альбумина и протеина С.
Портальная эмболизация
Необходимость выполнения обширных резекций печени больным с низким функциональным резервом или недостаточным объёмом остающейся после резекции паренхимы привела к необходимости поиска методик, позволяющих снизить риск развития пострезекционной печёночной недостаточности. С этой целью был разработан и с 1986 года активно используется метод дооперационной портальной эмболизации (рис. 59-15). Метод рассчитан на стимуляцию компенсаторной гипертрофии остающейся после резекции доли печени путём эмболизации воротной системы доли, поражённой опухолью.
Рис. 59-15. Рентгеноконтрастная портограмма после чрескожной чреспечёночной портальной эмболизации. После вмешательства контрастное вещество не поступает в дистальные отделы портального русла, окклюзированные введением биологической клеевой композиции.
Экспериментальными и клиническими работами было показано, что портальная эмболизация вызывает отчётливую гипертрофию неэмболизированной доли печени и повышает её функциональный резерв. При этом интенсивность компенсаторной гипертрофии неэмболизированной доли, которая продолжается в течение 6 недель после процедуры, выражена в максимальной степени в течение первых 2 недель (рис. 59-16).
Рис. 59-16. Компьютерная томограмма до (а) и после (б) портальной венозной эмболизации.
Для выполнения портальной эмболизации используют 2 доступа: наиболее часто применяемый чрескожный чреспечёночный и через v. ileocolica. Выполнение последнего предусматривает мини-лапаротомию с последующим введением полиэтиленового катетера размером 7F через вышеуказанную вену в воротную.
Портальная эмболизация легче переносится больными по сравнению с артериальной и не несёт в себе риска развития тяжёлых осложнений. Известны лишь единичные случаи гемобилии и образования субкапсулярной гематомы, которые удавалось разрешить с помощью консервативных мер. Возможно попадание эмболизирующего материала в портальную систему противоположной доли печени, не имеющее серьёзных последствий.
Выполнение обширных резекций печени после предварительно выполненной портальной эмболизации позволяет рассчитывать на существенно более лёгкое течение ближайшего послеоперационного периода. При этом отмечается отсутствие признаков тяжёлой пострезекционной печёночной недостаточности, в том числе и у больных с циррозом печени.
Резектабельная опухоль что это
а) Определение:
• Теоретически выполнение полной резекции позволяет вылечить пациента от рака легких
б) Лучевые признаки резектабельности рака легкого:
1. Основные особенности:
• Оптимальный диагностический ориентир: резектабельной опухоль может быть на стадии I-IIIA
• Размер: возможность выполнения резекции зависит не только от размера опухоли
2. Рентгенография:
о Солитарный узелок ( 3 см) о Лимфаденопатия корня легкого и средостения на стороне поражения:
— Утолщенные паратрахеальные полосы, объемное образование в аортолегочном окне, под бифуркацией трахеи, расширение средостения
о Рецидивирующая постобструктивная пневмония о Ателектаз может быть вызван инвазией бронха и (или) сдавлением последнего увеличенными лимфатическими узлами
3. КТ:
• КТ с контрастным усилением:
о Размер опухоли определяют по трем измерениям
о Оценка структуры опухоли (солидная, с изменениями по типу «матового стекла», смешанная-солидная с изменениями по типу «матового стекла», наличие кальция, жира)
о Установление локализации опухоли относительно плевры, средостения и бифуркации трахеи
о Оценка лимфатических узлов: при размере > 1 см в средостении или > 1,2 см под бифуркацией трахеи лимфатические узлы подозрительны на наличие метастазов О Выявление плеврального выпота, утолщения плевры (при ее контакте с опухолью на протяжении > 3 см следует подозревать инвазию плевры)
о При отсутствии визуализации пространств с жировой тканью следует подозревать вовлечение в опухолевый процесс грудной стенки или средостения
о Выявление отдаленных метастазов: в надпочечниках (40%), печени (30%), костях (20%), головном мозге (10%)
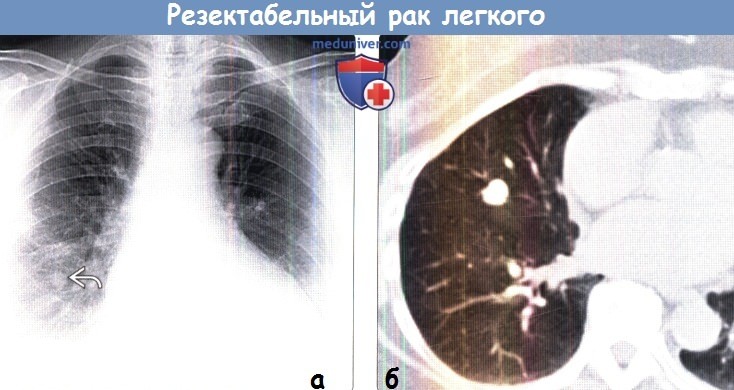
(б) У той же пациентки при нативной КТ было подтверждено наличие в средней доле правого легкого узелка. На томограмме лучше визуализируется его дольчатый контур.
При последующей ПЭТ/КТ (не изображена) узелок накапливал ФДГ, при этом признаков наличия метастазов выявлено не было. Картина соответствует клинической стадии IA (Т1а, N0, М0) рака легких.
При резекции средней доли правого легкого был подтвержден диагноз аденокарциномы. 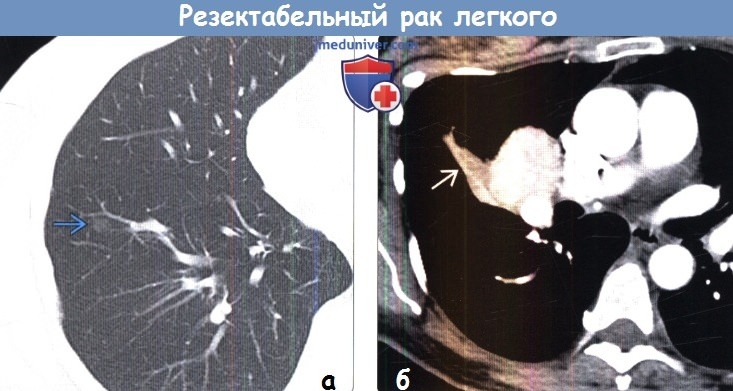
(б) У никогда не курившего пациента 52 лет с выраженным гемофтизом при КТ с контрастным усилением визуализируется объемное образование с дольчатым контуром размером 5 см, характеризующееся наличием кальцификатов. Образование обусловило развитие ателектаза средней доли.
При трансбронхиальной биопсии был подтвержден диагноз карциноидной опухоли. Поскольку опухоль соответствовала стадии IB (Т2, N0, М0), была выполнена лобэктомия. 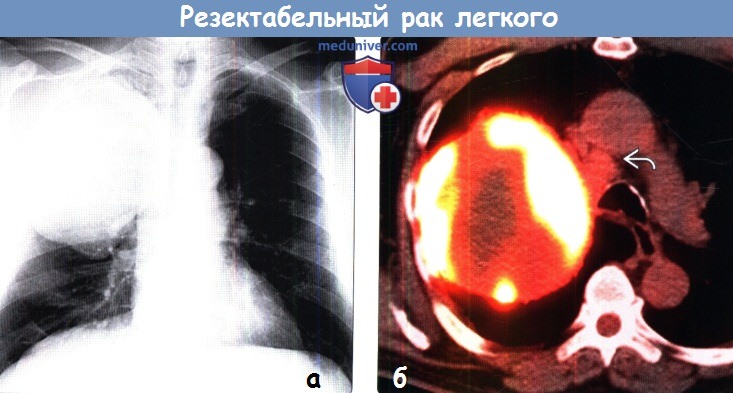
(б) У того же пациента при ПЭТ/КТ визуализируются выраженное накопление ФДГ периферическими отделами данной плоскоклеточной карциномы и наличие некроза в ее центре. Следует отметить умеренный уровень поглощения ФДГ нижним паратрахеальным лимфатическим узлом справа (4R).
Картина соответствует клинической стадии IIIA (Т3, N2, N0) рака легких.
Были выполнены правосторонняя верхняя лобэктомия, диссекция лимфатических узлов и химиотерапия.
4. Методы медицинской радиологии:
• ПЭТ/КТ:
о Часто выполняется для выявления отдаленных метастазов и оценки лимфатических узлов средостения в целях стадирования опухоли:
— Бессимптомные отдаленные метастазы были выявлены у 24% пациентов, которым по результатам первичного стадирования предполагалось выполнять хирургическое вмешательство
— Отсутствие визуализации интенсивно поглощающих ФДГ лимфатических узлов не является достаточным поводом для отказа от выполнения биопсии при медиастиноскопии или бронхоскопии
о Используется в послеоперационном периоде для выявления местного рецидивирования
о Ложноположительные результаты при воспалительных процессах
5. МРТ:
• Может выполняться при подозрении на инвазию миокарда, грудной стенки или диафрагмы
• Метод выбора для выявления метастазов в головном мозге
6. Рекомендации к проведению лучевых исследований:
• КТ представляет собой метод выбора для первичной оценки узелка в легочной ткани, а ПЭТ/КТ-для первичного клинического стадирования рака легких
в) Дифференциальный ряд заболеваний:
1. Аденокарцинома:
• Узелок, объемное образование солидное, частично солидное или с изменениями по типу «матового стекла»
• Контур спикулообразный, неровный или дольчатый
2. Плоскоклеточный рак:
• Объемное образование центральной локализации; образования периферической локализации могут характеризоваться наличием полостей
3. Мелкоклеточный рак:
• Крупное объемное образование центральной локализации, инвазирующее корень легкого и средостение и часто метастазирующее в лимфатические узлы
4. Карциноид бронха:
• Узелок или объемное образование центральной локализации с четким контуром, часто характеризующееся наличием опухолевого компонента в просвете бронха
г) Патоморфология:
1. Стадирование, определение степени дифференцировки и классификация опухолей:
• Применимо к НМРЛ, МРЛ и карциноиду бронха
2. Микроскопические особенности:
• В основе классификации лежит гистологический тип опухоли


д) Клинические аспекты резектабельного рака легкого:
1. Проявления:
• Наиболее частые признаки:
о Часто выявляют случайно методами лучевой диагностики
• Другие признаки:
о Кашель, одышка, ателектаз, хрипы, рецидивирующая постобструктивная пневмония
3. Лечение:
• НМРЛ на стадии I или II: резекция с диссекцией лимфатических узлов средостения и проведение в некоторых случаях адъювантной химиолучевой терапии:
о Предпочтительна резекция доли легкого, однако при низком пульмональном резерве может быть выполнена субдолевая резекция; может быть проведена в ходе видеоторакоскопии
о При опухолях на стадии Т3 часто необходимо выполнять пневмонэктомию
о При невозможности выполнения хирургического вмешательства проводятся облучение или чрескожная абляция
• НМРЛ на стадии IIIA: резекция обычно в сочетании с химиолучевой терапией
• МРЛ: на момент выявления обычно характеризуется наличием метастазов; системная терапия, хирургические вмешательства играют незначительную роль
е) Диагностические пункты:
• При случайном выявлении неопределенных узелков в легочной ткани следует заподозрить рак легких по причине его широкой распространенности и высокого уровня смертности от этого заболевания, особенно при опухолях на поздних стадиях
ж) Список литературы:
1. Boffa DJ et al: Now or later: evaluating the importance of chemotherapy timing in resectable stage III (N2) lung cancer in the National Cancer Database. Ann Thorac Surg. 99(1):200-8, 2015
Редактор: Искандер Милевски. Дата публикации: 27.1.2019


