Репликация что это в медицине
Репликация вирусов
Репликация вирусов
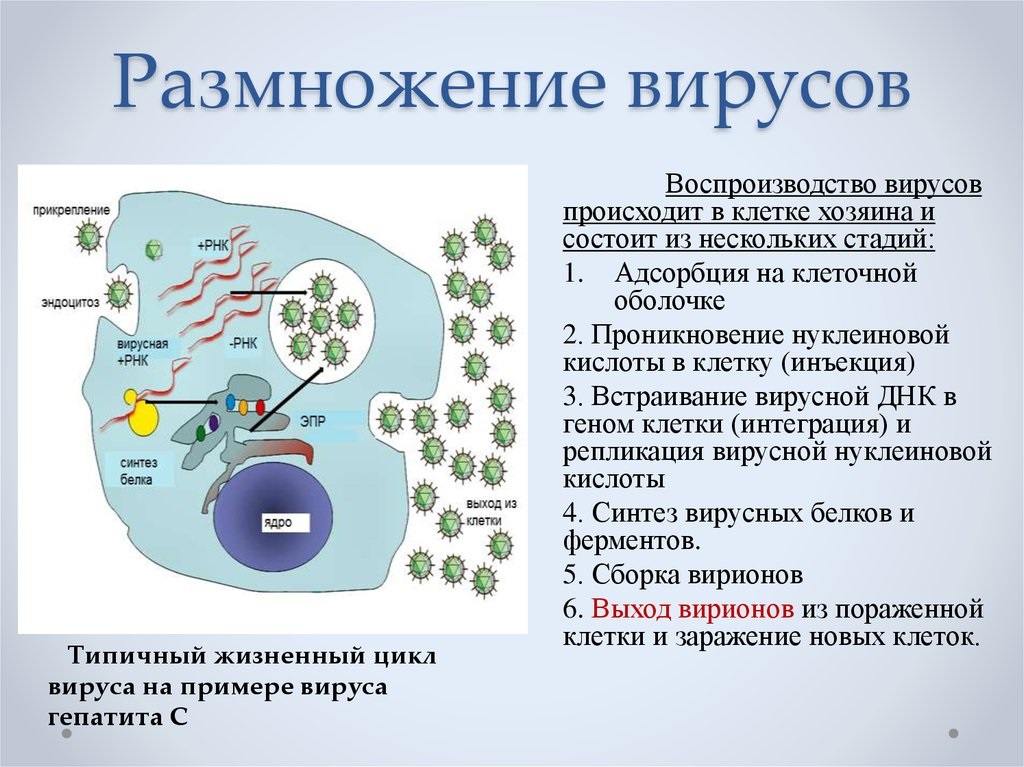
Размножение вируса, или репликация, является весьма характерным процессом, свойственным только обитателям этого особого мира природы. Как известно, рост организмов растительного и животного мира природы невозможен без деления клеток. Вирус же вообще не увеличивается в размерах. Вирусные частицы появляются сразу «взрослыми» в результате своеобразного процесса, названного репликацией. Но самое поразительное — то, что в продуцировании новых вирусных частиц участвует только одна нить: одинарная цепочка нуклеиновой кислоты.
Проследим за нуклеиновой кислотой бактериофага, проникшей в клетку бактерии. Первым делом ДНК выключает жизненно важные для клетки хозяина процессы. Затем начинают образовываться специфические вещества ферменты, идущие на строительство молекул ДНК, точно таких же, какие были и у бактериофага. Примерно через 8 мин образование ферментов замедляется и начинают образовываться белки капсидов. На строительство цепочек нуклеиновых кислот потомства кроме ферментов идет часть родительской ДНК бактериофага и разбитая ДНК хозяина. Капсиды новых бактериофагов строятся из вновь образованных белков; сюда же идет часть белков разрушенной клетки и старого бактериофага.
Примерно через 15 мин после инфицирования в клетке бактерий образуется столько вирусных частиц, что им становится тесно. Они разрывают оболочку хозяина и вырываются наружу, заражают новые клетки бактерий и т. д.
Репликация вирусов как сборочный конвейер
Часто процесс репликации вирусов сравнивают с заводским сборочным конвейером, действующим по заранее разработанному технологическому процессу. Сначала под руководством ДНК идет изготовление строго определенных элементов деталей. Далее ДНК вырабатывает белки своей сферы и ядрышко, вокруг которого белки под влиянием электростатических сил собираются в сферу. Ядрышко уничтожается, после того как образовалась головка-сфера. Один из ответственейших моментов сборки — заполнение сферы цепочкой ДНК. К этому моменту из отдельных участков «цеха сборки» к «главному конвейеру» подаются недостающие детали бактериофага: стержень, сократительные кольца, пластинки, нити. Эти детали друг за другом прикрепляются к сфере.
Интересно, что «рабочие» операции по сборке вирусов сходны с процессами зарождения и развития более сложных организмов. Не заимствованы ли эти приемы из мира вирусов?
Кстати, технические приемы репликации различных видов вирусов не только состоят из общих операций, но имеют и некоторые особенные черты. Так, вирусы оспы размножаются в цитоплазме, а вирусы группы герпеса и аденовирусы — в ядре. В процессе построения нуклеиновых кислот участвуют разрушенные системы клетки хозяина. Следовательно, вирусам оспы и аденовирусам придется использовать различный строительный материал. Эти вирусы относятся к группе крупных вирусов. Например, в молекуле ДНК вируса осповакцины закодировано около 500 белков. Цикл размножения длится более 20 ч. Можно представить, как сложно контролировать процесс репликации вируса! И если системы, отвечающие за последовательность сборки, хоть раз ошибутся, вирусу не удастся «самособраться». Запомните это уязвимое место в процессе репликации.
Репликация что это в медицине
Репликация митохондриальной и ядерной ДНК происходит в разные фазы клеточного цикла. Несмотря на то что общая последовательность стадий при репликации ядерной ДНК у высших существ (эукариот) и у бактерий (прокариот) одинакова, сам процесс имеет незначительные отличия. Так, у эукариот во время репликации ДНК (ядерная) остаётся в нуклеосомной конфигурации.
Фрагменты ДНК, богатые парами оснований Г—Ц (R-полосы эухроматина в уплотнённом хроматине), экспрессируют гены «домашнего хозяйства», которые функционируют во всех клетках организма. Данные фрагменты реплицируются на ранней стадии S-фазы. Участки гетерохроматина, богатые парами оснований А—Т (G-полосы), экспрессируют небольшое количество генов и реплицируются на поздней стадии S-фазы.
Гены с большим содержанием пар А—Т, кодирующие различные свойства и функционирующие лишь в определённых клетках, входят в состав факультативного гетерохроматина. Их репликация происходит на ранней стадии S-фазы только в тех клетках, в которых они экспрессируются, и на поздних стадиях — в клетках, где экспрессии не происходит.
Область спирали ДНК, которая в начале репликации раскручивается в первую очередь, называют участком начала репликации (репликоном). В этом месте двойную нить расплетает фермент хеликаза, раскрывающий последовательность оснований. Процесс репликации происходит вдоль одной цепи со скоростью примерно 40-50 нуклеотидов в секунду одновременно в обоих направлениях. У высших существ имеется множество репликонов, расположенных на расстоянии 50 000—300 000 п.н. В месте разделения нити ДНК возникают репликационные вздутия, на каждом конце которого формируется репликационная вилка.
Новая ДНК синтезируется при участии ферментов, называемых ДНК-полимеразами, из дезоксирибонуклеотидтрифосфатов (АТФ, ГТФ и др.), которые превращаются в монофосфатные нуклеотиды (АМФ, ГМФ и др.). Отщепление и гидролиз пирофосфатов из трифосфатов обеспечивают процесс энергией и обусловливают его полную необратимость, делая молекулу ДНК достаточно устойчивой.
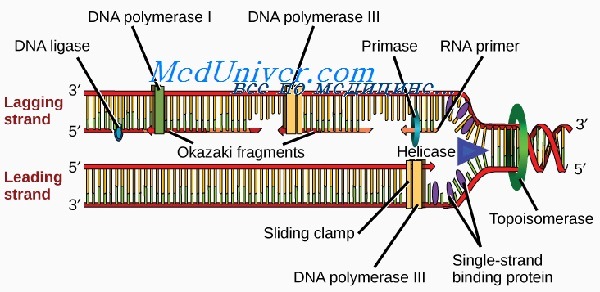
Все ДНК-полимеразы могут выстраивать новую ДНК только в направлении от 5′- к 3′-концу. Это означает, что ферменты должны двигаться вдоль матричной цепи от 3′- к 5′-концу. В связи с этим репликация может непрерывно происходить от репликона только по одной цепи, называемой опережающей. Из-за расположения Сахаров репликация по второй, отстающей цепи происходит только на коротких отрезках, известных как фрагменты Оказаки.
Длина новых фрагментов ДНК, образующихся вдоль отстающей цепи, в среднем составляет 100—200 пар нуклеотидов. Во время синтеза фрагменты Оказаки сшивает между собой фермент ДНК-лигаза. В ожидании репликации стабильность первичной одноцепочечной нуклеотидной последовательности отстающей цепи поддерживается белком, связывающим одноцепочечную ДНК (или спиральдестабилизирующим белком).
Для синтеза опережающей цепи необходим фермент ДНК-полимераза S, а для синтеза отстающей — ДНК-полимераза а. Последняя имеет субъединицу, называемую ДНКпраймазой, которая синтезирует короткую РНК-затравку, играющую роль праймера. Репликация мито-хондриальной ДНК происходит независимо от процессов в ядре. При этом используется ряд других ферментов, один из которых — ДНК-полимераза у.
В геноме присутствует большое количество копий пяти гистонных генов, благодаря чему происходит синтез множества гистонов (особенно во время S-фазы), которые сразу после репликации связываются с новой цепью ДНК.
Следует отметить, что процесс репликации носит название полуконсервативного, так как в состав дочерних молекул ДНК входит одна первичная цепь и одна синтезированная.
Репликация теломер ДНК
Основной проблемой синтеза ДНК на конце отстающей цепи служит то, что ДНК-полимеразе а необходимо прикрепиться выше конца последовательности, которая реплицирована, и работать проксимально в направлении от 5′- к 3′-концу. Для решения этой проблемы нужен ДНК-синтетический фермент теломераза, который продлевает отстающую цепь.
Теломераза — рибонуклеопротеин, содержащий матричную РНК с последовательностью 3′-ААУЦЦЦААУ-5′, которая комплементарна полутора повторам шестиосновной теломерной ДНК (5′-ГГГТТА-3′). Фрагмент последовательности 3′-ААУ РНК-теломеразы связывается с терминальным концом ТТА-5′ матричной отстающей цепи, при этом остальная часть РНК остаётся свободной. Затем к этой матричной РНК присоединяются дезоксирибонуклеотиды, тем самым продлевая повторяющуюся последовательность в ДНК на один сегмент.
После этого теломераза отщепляется и направляется к другому терминальному концу с последовательностью ТТА-5′, и процесс повторяется. Как только возникает достаточно длинный терминальный повтор, ДНК-полимераза а прикрепляется к полученному одноцепочечному фрагменту и достраивает вторую цепь по методу комплементарности в проксимальном 5’—3′-направлении, двигаясь к уже существующему двухцепочечному участку, последующее слияние с которым происходит благодаря действию ДНК-лигазы.
Репаративные механизмы ДНК
Иногда в растущую цепь случайно вклинивается неправильное основание, однако, к счастью, у здоровых клеток присутствуют пострепликационные репаративные ферменты и система коррекции ошибочного спаривания оснований, которые исправляют подобные ошибки. В основе механизма действия данных систем лежат удаление и замена ошибочно вставленных оснований в соответствии с последовательностью матричной цепи. Для их функционирования необходимы ДНК-полимеразы b и е.
Значение ДНК для медицины. Патология пострепликационных механизмов репарации иногда обусловливает предрасположенность пациентов к некоторым онкологическим заболеваниям. К ним относят синдром множественной ломкости хромосом (синдром Блума), наследственную предрасположенность к раку молочной железы, вызванную мутациями генов BRCA1 и BRCA2, и аутосомно-доминантную форму рака кишечника (наследственный неполипозный рак толстой кишки).
Существует теория, утверждающая, что после каждого клеточного цикла теломеры укорачиваются на один повтор, а следовательно, количество делений клетки ограничено числом повторов в теломерной цепи. Согласно этому бесконечный рост и деление опухолевых клеток происходят из-за присутствия активных мутантных теломераз, которые препятствуют разрушению теломер.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в содержание раздела «генетика» на нашем сайте
РЕПЛИКАЦИЯ
Репликация (позднелат. replicatio повторение; син. редупликация) — процесс биосинтеза молекул дезоксирибонуклеиновых кислот, в результате к-рого из одной молекулы образуются две дочерние, полностью идентичные материнской. Репликация дезоксирибонуклеиновых кислот (см.) обеспечивает передачу полного комплекса наследственной генетической информации от поколения к поколению (см. Наследственность). Свойство молекул ДНК редуплицироваться проявляется и в репродукции хромосом (см.) высших организмов.
Согласно модели, предложенной Дж. Уотсоном и Ф. Криком, молекула ДНК представляет собой двойную спираль, построенную из комплементарных друг другу цепей дезоксирибонуклеотидов. В процессе Репликации водородные связи между парами нуклеотидов разрываются и к ним присоединяются новые, комплементарные соответствующим дезоксирибонуклеотидам дезоксинуклеозидтрифосфаты. Процесс соединения нуклеотидов в полинуклеотидную цепь происходит с отщеплением пирофосфата. Репликация ДНК носит характер полуконсервативного процесса, т. е. каждая дочерняя двойная спираль включает в себя одну материнскую и одну вновь синтезированную полинуклеотидную цепь.
Образованию вилки репликации предшествует взаимодействие с молекулой ДНК особого белка (ДНК-раскручивающего белка), устраняющего суперспиральные витки и локально раскручивающего двойную спираль ДНК. Предполагают, что ДНК-раскручнвающий белок встраивается в дезоксирибозофосфатную цепь. Эта реакция обратима: после высвобождения ДНК-раскручивающего белка спиральная структура ДНК восстанавливается. Локальное расхождение комплементарных цепей ДНК обеспечивают белки-дестабилизаторы двойной спирали ДНК. Присоединяясь к ДНК, белки-дестабилизаторы снижают термостабильность ее молекулы, к-рая приобретает способность плавиться при температуре на 40° ниже обычной температуры плавления.
Рост новой цепи ДНК в вилке репликации катализируется ферментом ДНК-полимеразой (см. Полимеразы). В клетках высших организмов и бактерий обнаружено несколько форм ДНК-полимераз, но Р. генома у эукариотов осуществляется только под действием ДНК-полимеразы а, а у бактерий — ДНК-полимеразы III. Комплементарные цепи двойной спирали ДНК антипараллельны по ориентации углеродных атомов дезоксирибозы (см.). Следовательно, при движении вилки репликации одна дочерняя цепь должна нарастать в направлении 5′ —> 3′, а другая — в направлении 3′ —> 5′. Вместе с тем все ДНК-полимеразы способны присоединять новые нуклеотиды только к З’-гидроксильной группе дезоксирибозы растущей цепи ДНК, тем самым обеспечивая синтез только в направлении 5′ —> 3′, т. е. первым образуется 5′-конец новой цепи. Сама ДНК-полимераза к тому же не способна инициировать синтез новых цепей на одноцепочечной ДНК-матрице. Было установлено, что обе эти трудности преодолеваются путем синтеза на одной цепи коротких полинуклеотидных фрагментов с полярностью 5′ —> 3′ в направлении, противоположном движению вилки репликации (рис. 2). При этом инициацию Р. каждого нового фрагмента ДНК осуществляет фермент РНК-полимераза (так наз. примаза), при участии к-рого на ДНК-матрице синтезируется инициатор (затравка) — короткий участок РНК (так наз. РНК-праймер), к 3′-гидроксильной группе рибозы к-рого ДНК-полимераза начинает присоединять дезоксирибонуклеотиды. Впоследствии РНК-праймер удаляется экзонуклеазой (см. Нуклеазы), а образовавшаяся брешь закрывается ДНК-полимеразой. У Escherichia coli 5′ —> З’-экзонуклеазной активностью обладает ДНК-полимераза I.
Отдельные полинуклеотидные фрагменты сшиваются между собой ферментом ДНК-лигазой (КФ 6.5.1.1; 6.5.1.2). При этом одна из двух цепей ДНК растет непрерывно (ведущая нить), а другая — прерывисто (запаздывающая нить). Фрагменты прерывистого синтеза ДНК называют фрагментами Окадзаки (Оказаки) по имени открывшего их японского ученого Окадзаки (R. Okazaki). У бактерий фрагменты Окадзаки имеют длину ок. 1000 нуклеотидных пар, а их РНК-праймер — 50—200 нуклеотидных пар. У высших организмов фрагменты Окадзаки состоят приблизительно из 150—200 нуклеотидных пар, а их РНК-праймер — из 10—20 пар.
Присоединив очередной нуклеотид к растущей цепи ДНК, ДНК-полимераза «сверяет» его с партнером на цепи-матрице, и в случае несоответствия паре (А — Т или Г — Ц) та же полимераза проявляет 3′ —> 5′-экзонуклеазную активность, удаляя ошибочно присоединенный нуклеотид. Т. о. осуществляется коррекция, обеспечивающая высокую точность процесса Р. молекул ДНК, что определяет сохранность наследственной информации в ряду поколений клеток и организмов.
В клетках, размножающихся путем митоза (см.), и у бактерий репликация ДНК происходит между актами деления клеток; в мейозе (см.) ДНК редуплицируется один раз перед двумя следующими друг за другом делениями, что приводит к редукции (уменьшению) вдвое количества ДНК (как и числа хромосом) на клетку. Этот отрезок интерфазы называют периодом синтеза ДНК или S-периодом.
Репликацияначинается (инициируется) в определенных участках молекулы ДНК (по терминологии Ф. Жакоба — репликаторах), первичная структура к-рых характеризуется высоким содержанием пар А — Т и наличием так наз. обратных повторов (палиндромов). От точки инициации движутся либо одна, либо две вилки репликации (в последнем случае они движутся в противоположные стороны), обеспечивая элонгацию (удлинение) вновь синтезирующихся участков молекулы ДНК. Терминация (окончание) Р. происходит либо при слиянии двух вилок репликации, двигающихся навстречу друг другу, либо в специальных точках терминации Р.
Отрезок молекулы ДНК, реплицирующийся в результате одного акта инициации, называют единицей репликации или реплпконом. В геноме бактерий, как правило, имеется всего один участок инициации Р., связанный с клеточной мембраной. Кольцевая молекула ДНК генома бактерии реплицируется как один репликон. В геноме эукариотов Р. осуществляется полирепликонно, т. е. инициация Р. происходит одновременно во многих точках по длине молекул ДНК. Установлено, что на молекулах ДНК генома эукариотов имеется большое число потенциальных точек инициации Р., расположенных на расстоянии 1—4 мкм друг от друга. В зависимости от того, сколько потенциальных точек инициации вовлечены в Р., может меняться размер репликона. Напр., при репликации ДНК в дробящихся яйцах дрозофилы, где деления клеток следует очень быстро одно за другим, в Р. включается каждая вторая или третья потенциальная точка Р. и размер репликации равен 9—12 мкм; при удвоении ДНК соматических клеток эукариотов в Р. участвует в среднем 1 из 10 или даже из 100 потенциальных точек инициации Р. и размер репликонов увеличивается до 30—300 мкм.
Репликация ДНК вирусов в основном сходна с репликацией ДНК высших животных и бактерий; она осуществляется ферментами клетки хориона. В нек-рых случаях (вирусы герпеса) РНК-затравка обнаруживается в составе вирионной ДНК. У онкогенных ДНК-содержащих вирусов (паповавирусы) ДНК может интегрировать в геном клетки, после чего репликация вирусной ДНК происходит вместе с ДНК клетки.
Репликация большинства РНК-содержащих вирусов осуществляется вирусспецифическими ферментами — РНК-зависимыми РНК-полимеразамн (репликазы), к-рые достраивают комплементарную нить на вирионной РНК-матрице, образуя так наз. репликативные формы РНК.
У онкогенных РНК-содержащих вирусов (см. Ретровирусы) Р. осуществляется ферментом РНК-зависимой ДНК-полимеразой (обратная транскриптаза, ревертаза), к-рый синтезирует ДНК-копию вирусного генома, способного встраиваться в геном клетки (см. Вирусы).
У бактерий и эукариотов, как правило, в каждом цикле деления клеток должна реплицироваться вся ДНК и при этом только один раз. Это значит, что должны существовать регуляторные системы, контролирующие инициацию Р. и отличающие родительские и дочерние молекулы. Механизм такой регуляции пока не ясен.
В определенных случаях (в норме и при патологии) может происходить многократная Репликация всего генома без последующего деления клетки (это приводит к возникновению полиплоидных ядер ) или Р. отдельных частей генома без Р. всего генома, так наз. экстрарепликация (напр., амплификация ДНК рибосомного гена в оогенезе нек-рых животных). Описаны случаи недорепликации части ДНК генома в клетках эукариотов. Это касается только ДНК гетерохроматина, в к-ром нет генов, необходимых для жизнеобеспечения клетки.
Сходство ферментов Репликации и основных процессов, происходящих в вилке репликации, у прокариотов и эукариотов свидетельствует о высокой эволюционной стабильности и жестком генетическом контроле процесса репликации ДНК. Нарушения нормального процесса Репликации влияют на деление и могут привести к гибели клеток.
Библиография: Бостон К. и Самнер Э. Хромосома эукариотической клетки, пер. с англ., с. 248, М., 1981; Корнберг А. Синтез ДНК, пер. с англ., М., 1977; Уотсон Д ж. Молекулярная биология гена, пер. с англ., М., 1978; DNA synthesis, ed. by J. Molineux a. M. Kohiyama, N. Y.— L., 1978; Jacob F., Brenner S. a. Сuzin F. On the regulation of DNA replication in bacteria, Cold Spr. Harb. Symp. quant. Biol., v. 28, p. 329, 1963.
Чем лечат коронавирус: 8 перспективных препаратов
Как сообщил РБК Виктор Малеев, советник НИИ эпидемиологии Роспотребнадзора, пока в мире не созданы эффективные средства и для лечения коронавируса врачи применяют комбинации существующих. Каких именно, Минздрав уточнил в списке рекомендованных препаратов. В их число вошли гидроксихлорохин, интерферон, лопинавир и ритонавир.
В начале сентября Минздрав выпустил обновленную, восьмую версию рекомендаций по профилактике, диагностике и лечению новой коронавирусной инфекции COVID-19. Доступная инфографика опубликована на сайте министерства.
Как отмечают эксперты, для профилактики коронавируса можно использовать препараты умифеновир, рекомбинантный интерферон альфа (ИФН-α). После контакта с зараженным SARS-CoV-2 нужно принимать гидроксихлорохин.
Материал прокомментировала и проверила Поленова Наталья Валерьевна, кандидат медицинских наук, семейный врач, кардиолог, детский кардиолог, диетолог GMS Clinic.
Что известно о COVID-19
COVID-19 — инфекционное заболевание, которое вызывает коронавирус SARS-CoV-2. Обнаруженный в Китае в конце 2019 года, к 15 мая он поразил 4,4 млн человек во всем мире. Большинство тех, у кого выявлены симптомы, жалуются на высокую температуру, кашель и затрудненное дыхание. Специальные лекарства и вакцины против COVID-19 пока не разработаны. Однако вирусолог, руководитель лаборатории геномной инженерии МФТИ Павел Волчков сообщил, что первое эффективное средство от коронавирусной инфекции может появиться осенью.
В целом для лечения коронавируса Минздрав рекомендует использовать шесть лекарств. это фавипиравир, ремдесивир, умифеновир, гидроксихлорохин, азитромицин и интерферон альфа.
Гидроксихлорохин и мефлохин
Препаратами на основе хлорохина врачи уже больше 70 лет лечат малярию и аутоиммунные заболевания (например системную красную волчанку). Ученые обнаружили, что активное вещество эффективно и против вируса SARS-CoV-2. В марте китайский холдинг Shanghai Pharmaceuticals предоставил России для лечения COVID-19 препарат гидроксихлорохин (производное хлорохина). Минздрав не выявил противопоказаний и разрешил применение, передав в больницы более 68 тыс. упаковок, несмотря на то что в России гидроксихлорохин не зарегистрирован.
Ученые до сих пор спорят, насколько обосновано применение гидроксихлорохина. Исследования французского инфекциониста Дидье Рауля показали положительные результаты. Но Associated Press опубликовало данные американских исследований. Анализ историй болезни пациентов, которых лечили при помощи препарата, показал, что гидроксихлорохин помогает хуже, чем стандартные средства.
Федеральное медико-биологическое агентство РФ в апреле провело клинические испытания мефлохина (утвержденный в России аналог гидроксихлорохина). Ученые выясняли, насколько этот противомалярийный препарат эффективнее и безопаснее. По предварительным данным исследования с участием 347 пациентов, после применения мефлохина в 78% случаев отмечена положительная динамика. Окончательные выводы ФМБА предоставит в конце мая.
Лопинавир и ритонавир
Комбинация противовирусных средств под названием калетра используется для лечения ВИЧ. По данным ВОЗ, применение средства в сочетании с другими лекарствами эффективно при борьбе с коронавирусом. В конце января Минздрав включил лопинавир с ритовинаром в список препаратов, рекомендуемых при COVID-19 в качестве противовирусной терапии. В результате спрос и продажа калетры выросли в десятки раз. Эксперты предупреждают, что бесконтрольный прием средства без назначения врача может причинить вред здоровью, в том числе вызвать диарею и поражения печени.
Китайские ученые обнаружили, что лопинавир и ритонавир не эффективны при лечении легкой или средней стадии COVID-19. Прием препаратов не улучшает клиническую картину, более того, может вызывать побочные эффекты. В эксперименте участвовали 86 пациентов, из них 34 человека принимали комбинацию лопинавира и ритонавира, а 17 больных не получали никаких препаратов. Спустя две недели обе группы показали аналогичные результаты, но те, кто принимал лекарства, испытывали побочные эффекты.
Ремдесивир
Ремдесивир применяют для лечения лихорадки Эбола. Канадские ученые из Университета Альберты выяснили, что препарат блокирует размножение коронавируса. Исследования доказали эффективность противовирусного средства при лечении респираторного синдрома MERS и атипичной пневмонии SARS-CoV, структура РНК которых аналогична коронавирусу. Вирусологи получили идентичные результаты в случае с SARS-CoV-2, вызывающим COVID-19, и пришли к выводу, что ремдесивир можно использовать для лечения. New England Journal of Medicine также опубликовал результаты исследования, в ходе которого применение препарата улучшило состояние 68% пациентов. Премьер-министр Японии Синдзо Абэ 28 апреля заявил в парламенте, что планирует разрешить использование ремдесевира для лечения COVID-19. В США препарат прошел успешные испытания, и 2 мая Управление по санитарному надзору экстренно выдало разрешение на его применение.
APN01
Австрийская биотехнологическая компания APEIRON Biologics AGН начала клинические испытания препарата APN01, который был разработан в начале 2000-х годов. Ученые обнаружили, что белок ACE2, входящий в его состав, подавляет инфекции, вызванные вирусами группы SARS. А также помогает защитить легкие при дыхательной недостаточности.
Власти Австрии, Германии и Дании согласились провести клинические испытания препарата. В ходе исследований 200 пациентов с COVID-19 получат APN01. Затем вирусологи оценят действие средства, а также проанализируют его эффективность и безопасность для больных, которым необходима искусственная вентиляция легких.
Фавилавир (фавипиравир)
Китайские врачи одобрили для лечения COVID-19 противовирусный препарат фавилавир (фавипиравир). Это средство применяют при воспалениях органов дыхательной системы. Результаты исследований, проведенных среди 70 человек, пока не опубликованы, но препарат, как утверждают вирусологи, доказал эффективность.
В феврале фармацевтическая компания Zhejiang Hisun Pharmaceutical получила разрешение на продажу фавипиравира как потенциального лекарства от коронавируса.
Рибавирин
Оценить эффективность и безопасность рибавирина достаточно сложно. С одной стороны, это средство угнетает размножение подавляющего большинства вирусов, с другой — механизм действия рибавирина до конца не изучен. В конце января Минздрав рекомендовал использовать это противовирусное средство для лечения коронавируса. Детям его назначают при респираторно-синцитиальной инфекции (редкая разновидность ОРВИ), которая вызывает тяжелое поражение легких. Препарат применяют при тяжелом гриппе, у детей с иммунодефицитом — при кори, а в сочетании с интерфероном рибавирином лечат вирусный гепатит С.
Однако академик РАН Александр Чучалин раскритиковал рекомендации Минздрава. При назначении препарата взрослым необходимо учитывать его тератогенность (угрозу нарушения эмбрионального развития), поэтому рибавирин категорически противопоказан при беременности. Несмотря на то что средство угнетает размножение многих вирусов, оно очень токсично и вызывает множество побочных эффектов.
В конце марта Минздрав исключил рибавирин из списка рекомендованных лекарств для лечения COVID-19.
Ивермектин
Австралийские ученые из университета Монаша и Королевского госпиталя в Мельбурне обнаружили антипаразитарное средство, которое в течение 48 часов практически уничтожает вирус SARS-CoV-2, уменьшая его присутствие на 99%. По мнению исследователей, применение ивермектина поможет избежать тяжелых осложнений COVID-19, а также предотвратить распространение вируса. В ходе опытов в зараженные SARS-CoV-2 клетки добавляли ивермектин. Через 24 часа доля вирусных РНК снижалась на 93%, а спустя 48 часов присутствие вируса уменьшалось на 99%.
Однократная обработка ивермектином способна за 48 часов вызывать уменьшение вируса в 5 тыс. раз, утверждают ученые. Препарат одобрен ВОЗ.
Нелфинавир
В комбинации с другими противовирусными препаратами нелфинавир используют для лечения ВИЧ. Исследование проводили японские ученые. Согласно полученным данным, препарат способен блокировать размножение SARS-CoV-2. Вирусологи исследовали девять аналогичных средств и обнаружили, что нелфинавир эффективен даже в небольших дозах. Поэтому его рекомендуют включить в перечень потенциально эффективных препаратов для лечения COVID-19.
Что делать, пока нет вакцины
Комментарий эксперта
Какие лекарства, кроме противовирусных препаратов и антибиотиков, рекомендованы для лечения COVID-19 Минздравом РФ?
Согласно восьмой версии постановления «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19) Минздрава РФ, пациенты, инфицированные вирусом SARS-CoV-2, должны получать при необходимости патогенетическую и поддерживающую симптоматическую терапию. К первой группе препаратов относятся, в первую очередь: глюкокортикостероиды (ГКС), ингибиторы интерлейкинов (тоцилизумаб, канакинумаб), антикоагулянты (эноксапарин, фраксипарин).
Глюкокортикостероиды способны предупреждать высвобождения цитокинов, веществ, отвечающих за развитие бурной воспалительной реакции, которая может привести очень опасному осложнению «цитокиновому шторму». ГКС могут быть полезны в лечении тяжелых форм COVID-19 для предотвращения необратимого повреждения тканей и неконтролируемой полиорганной недостаточности.
Следует отметить, что при легкой и средней степени тяжести течения заболевания, то есть пациентам, не получающих кислород, ГКс не показаны. Так что скупать гормоны из аптек для применения дома нет ни малейшей необходимости.
Препараты из группы ингибиторов цитокинов применяются при поражении паренхимы легких более чем на 50%, то есть стадия КТ-3, КТ-4 в сочетании с признаками нарастания интоксикации: длительно существующая лихорадка, очень высокие уровни воспалительных маркеров в крови.
В группах пациентов высокого риска тромбообразования для профилактики, так называемых, коагулопатий, целесообразно назначение антикоагулянтов, применяемых подкожно. Доказательств эффективности пероральных антикоагулянтов при COVID-19 пока недостаточно, однако, если пациент принимал их до заболевания, до прием препарата необходимо продолжить. К группам высокого риска относятся пациенты с сердечно-сосудистой патологией, сахарным диабетом, ожирением.
Как проводится симптоматическая терапия коронавируса?
К препаратам симптоматической терапии COVID-19 относят жаропонижающие лекарства, противокашлевые препараты, улучшающие отхождение мокроты. Наиболее безопасным жаропонижающим препаратом признан парацетамол.
Нет необходимости дожидаться определенного уровня лихорадки для применения жаропонижающего средства. При наличии головной и мышечной боли, плохой переносимости симптомов интоксикации и лихорадки, возможно применение препаратов и при относительно невысокой температуре тела.
Что можно принимать для профилактики коронавируса?
Важнейшими характеристиками рациона, способствующего укреплению иммунитета являются: адекватная суточная калорийность, достаточное потребление белка и ряда микронутриентов, в особенности, витамина С, Д, А, железа и цинка, повышение потребление пищевых волокон и, при необходимости, пробиотиков, соблюдение водного баланса. Согласно клиническим рекомендациями Российской Ассоциации эндокринологов, для профилектики дефицита витамина D у взрослых в возрасте 18-50 лет рекомендуется получать не менее 600-800 МЕ витамина в сутки. Людям старше 50 лет — не менее 800-1000 МЕ витамина D в сутки.
Существуют некоторые косвенные признаки потенциального противовирусного эффекта цинка против COVID-19, хотя их биомедицинские актуальность еще предстоит изучить. С учетом последних данных о клиническом течение болезни, кажется, что цинк может обладать защитным действием против COVID-19 за счет уменьшения частоты пневмонии, предотвращения повреждения легких, вызванного аппаратами ИВЛ, улучшения антибактериального и противовирусного иммунитета, особенно у пожилых людей.
Аскорбиновая кислота (витамин C, АК) принимает участие в таких жизненно важных физиологических процессах, как продукция гормонов, синтез коллагена, стимуляция иммунной системы и пр. Последний эффект может быть обусловлен как прямым противовирусным действием АК, так и ее противовоспалительными и антиоксидантными свойствами.