Ректальный катетер для чего
Катетеры Фолея: виды, особенности, применение
СОДЕРЖАНИЕ:
Для чего используются катетеры Фолея?
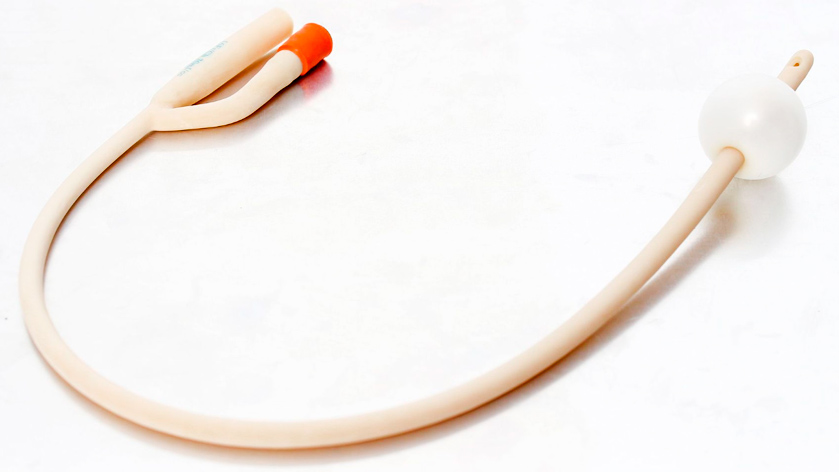
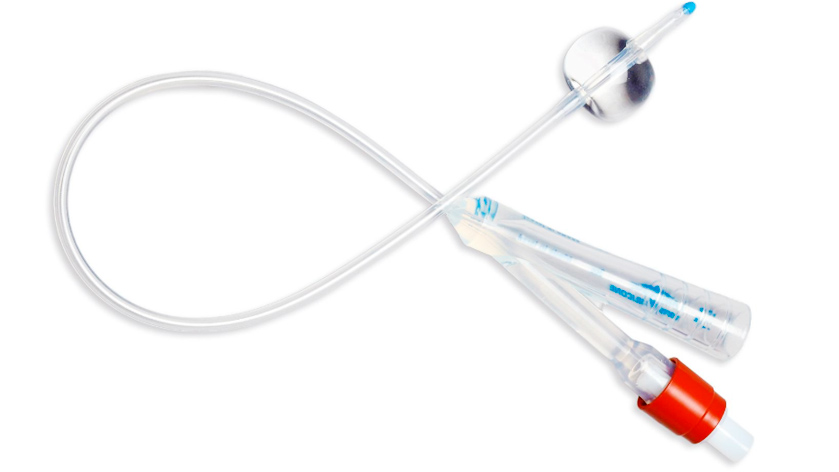
Латексные или силиконовые, трех- и двухходовые баллонные катетеры для длительной катетеризации мочевого пузыря.
Для чего используются катетеры Фолея?
Катетеры Померанцева-Фолея отличаются очень широкой сферой применения:
Использование катетеров Фолея при задержке мочеиспускания очень эффективно: отток мочи начинается уже в момент установки.
Катетеры такого типа чаще всего рекомендуются к установке пациентам, которые нуждаются в длительной катетеризации (от 5-7 до 30 суток)
Материал изготовления и конструкция катетера Фолея
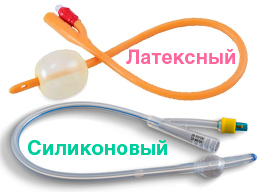
По материалу изготовления катетеры делятся на 3 типа:
Однако помимо материала, катетеры Фолея отличаются конструкцией и бывают 2 типов:
Строение урологического катетера Фолея:
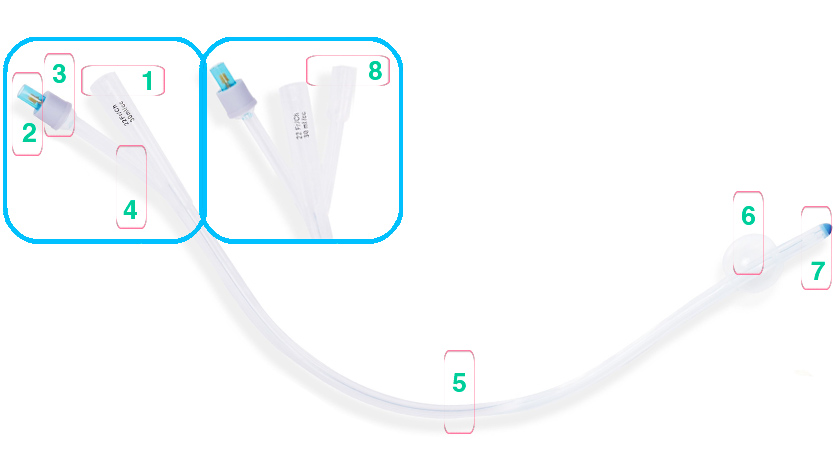 | 1. Отверстие для слива мочи |
| 2. Отверстие для наполнения баллона | |
| 3. Покрышка | |
| 4. Антирефлюксный клапан. | |
| 5. Трубка катетера | |
| 6. Баллон | |
| 7. Оливообразный наконечник с 2-я отверстиями для дренирования мочевого пузыря | |
| 8. Дополнительное отверстие для введения лекарственных средств. Есть только у трехходовых катетеров |
Виды катетеров Фолея
Катетеры для длительной катетеризации мочевого пузыря подразделяются на 3 вида:
Латексные двухходовые катетеры Фолея Vogt Medical с силиконовым покрытием
Таблица размеров катетеров Фолея:
| Пол | Размер | Цвет | Внутренний диаметр | Внешний диаметр | Длина | Объем баллона |
| Детский | Ch 6 | 1,1 мм | 2,0 мм | 28 см | 3-5 мл | |
| Детский | Ch 8 | 1,7 мм | 2,7 мм | 28 см | 3-5 мл | |
| Детский | Ch 10 | 2,3 мм | 3,3 мм | 28 см | 3-5 мл | |
| Мужской, Женский | Ch 12 | 2,8 мм | 4,0 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 14 | 3,3 мм | 4,7 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 16 | 3,8 мм | 5,3 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 18 | 4,5 мм | 6,0 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 20 | 5,1 мм | 6,7 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 22 | 5,6 мм | 7,3 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 24 | 6,2 мм | 8,0 мм | 39-40 см | 30 мл | |
| Мужской, Женский | Ch 26 | 6,9 мм | 8,7 мм | 39-40 см | 30 мл | |
| Мужской | Ch 28 | 7,5 мм | 9,3 мм | 39-40 см | 30 мл | |
| Мужской | Ch 30 | 8,0 мм | 10,0 мм | 39-40 см | 30 мл |
Как подобрать катетер Фолея?
Если говорить о том, какой катетер Фолея лучше, то тут важно ориентироваться на показания и рекомендации врача. В первую очередь это зависит от длительности катетеризации (периодическая, временная или пожизненная, при которой пациент всегда нуждается в помощи для мочеиспускания). Также при подборе учитываются 3 аспекта:
Определить размер, необходимый конкретному пациенту, может лечащий врач. Не рекомендуется делать это самостоятельно, т.к. диаметр трубки подбирается исходя из размеров уретры и уретрального канала. Например, ее внешний диаметр может составлять 2,7 мм, при внутреннем в 1,7 мм, а может достигать 8,7 мм, тогда внутренний будет 6,9 мм.
Как происходит постановка катетера Фолея?
Для установки катетера медсестра или врач всегда предварительно дезинфицируют руки, все инструменты и половые органы пациента. Все манипуляции проводятся в стерильных перчатках. Перед началом введения катетера между ног пациента ставят лоток или кладут пеленку. Катетер из упаковки нужно доставать пинцетом и при необходимости смазать стерильным лубрикантом на водной основе.
Уход за катетером Фолея и его замена
Промывание катетера необходимо, т.к. это изделие многоразового использования. Перед начало промывания нужно вымыть руки с мылом и обработать их антисептиками. Затем:
Процедуру нужно повторить несколько раз, пока катетер не очистится. Затем соединить его с трубкой и убрать в стерильное место.
Замена катетера тоже важна: его нужно использовать не больше 5, максимум 7 дней. Дольше можно пользоваться только катетерами из силикона. Смена катетера происходит так:
Рекомендуемые в России производители катетеров Фолея
Где купить катетеры Фолея?
Урологические катетеры Фолея можно заказать в специализированном интернет-магазине Стерильно.com. Компания работает напрямую с официальными представителями в России, поэтому у нас вы получите только сертифицированную продукцию по цене от производителя.
Зонд ректальный
Ректальный зонд предназначен для устранения вздутия и освобождения кишечника от скопившихся газов. Его также используют для введения лекарств, дренажа кишки и некоторых других медицинских манипуляций.
Необходимость использования данного устройства для борьбы с метеоризмом часто возникает в постоперационный период у пациентов, перенесших хирургическое вмешательство на кишечнике, в области заднего прохода, а также при наличии факторов, провоцирующих ухудшение работы мышц сфинктера, что мешает газам отходить самостоятельно. Как правило, газоотводную трубку используют для отвода газов только в тех случаях, когда альтернативные методы не принесли необходимых результатов или из-за особого состояния пациента.
Ректальный зонд с баллонным катетером применяется для интраректального введения лекарств, а ректальная трубка с дренажным мешком – для сбора стула. Данное устройство также не предназначено для регулярного использования, его устанавливают только в случае необходимости, чтобы избежать возможных осложнений, таких как ректальная перфорация и снижение тонуса мышц сфинктера.
Конструкция ректальных зондов
Ректальная трубка состоит из следующих элементов:
Модели, предназначенные для ректального введения лекарств и орошения прямой кишки, оснащены коннектором. К нему можно присоединять шприц или резиновый баллон. После завершения процедуры баллон отсоединяется от зонда, не разжимая.
Инновационные ректальные катетеры, используемые для ведения ЛС системного действия через прямую кишку, оснащены:
Данные зонды являются аналогами урологических двухходовых катетеров Фолея, но в отличие от них, они предназначены для ректального введения.
Материалы для ректальных зондов и их свойства
До недавнего времени для отведения газов повсеместно использовались только многоразовые трубки, основным материалом которых является резина. Их применение сопряжено с риском инфицирования пациента, поскольку данный материал требует сложной и длительной обработки. К тому же, слизистая оболочка прямой кишки легко впитывает в себя любые вещества, поэтому к материалу, используемому при производстве ректальных трубок, предъявляются повышенные требования к содержанию токсичных веществ, фталатов. Кроме того, он должен быть гипоаллергенным и апирогенным.
Стерильные изделия однократного использования изготавливаются из имплантационно-нетоксичного поливинилхлорида (ПВХ ). Среди важных характеристик этого технологичного полимера можно выделить термопластичность. Трубка из ПВХ имеет достаточную жесткость, но при контакте с телом нагревается, становится более мягкой и гибкой. Данное свойство материала, используемого для производства одноразовых ректальных зондов, минимизирует риск нанесения травм во время проведения процедуры медперсоналом или лицом, осуществляющим уход за больным, и снижает неприятные ощущения для пациента. Установка такого катетера не причиняет боли и не вызывает дискомфорта.
Кроме того, одноразовые ректальные зонды изготавливают из биосовместимых материалов — латекса-каучука и силикона.
Размеры ректальных катетеров
Производители выпускают ректальные зонды разных размеров для всех категорий пациентов. Наружный диаметр катетера измеряется по шкале Шарьера (FR или Ch). На каждом одноразовом изделии предусмотрена унифицированная цветовая маркировка, соответствующая международному стандарту ISO.
Детские ректальные зонды имеют длину 200 мм и следующие размеры:
Взрослые зонды имеют длину 400 мм и размеры от СН12 до СН34:
Ректальный зонд выбирается в зависимости от возраста пациента (для новорожденных, детей, подростков, взрослых), массы тела и анатомических особенностей. Для взрослых чаще всего подходят зонды 16 и 17 размера. От правильно подобранного размера изделия зависит качество выведения газов. Более широким зондом можно травмировать слизистую оболочку прямой кишки. Сложным осложнение неправильного использования зонда является ректальная перфорация.
Постановка Газоотводной трубки
Постановка ректального зонда проходит в несколько этапов:
Стерильная индивидуальная упаковка одноразовых ректальных зондов
На завершающем этапе производства готовые ректальные зонды обязательно стерилизуются в газовой камере. Ее наполняют окисью этилена с помощью вакуумного насоса. Газ за полчаса, в течение которых изделия находятся в камере, убивает все микроорганизмы.
Стерильная упаковка позволяет повысить качество ректальных зондов в процессе транспортировки и хранения на протяжении всего срока годности, который составляет 5 лет от даты производства.
Перед проведением любых манипуляций с использованием ректальной трубки необходимо проверить:
Выбор ректального зонда
Компания Главмед предлагает большой ассортимент ректальных зондов, размеры которых соответствуют международным стандартам ISO, что позволяет подобрать подходящую трубку для любого пациента – от новорожденных до пожилых людей. Мы реализуем медицинскую продукцию только проверенных производителей, качество которой не вызывает сомнений. Каждое изделие для ректальных процедур стерильно и находится в герметичной упаковке. Благодаря цветовой кодировке можно визуально определить диаметр трубки.
ООО Главмед имеет многолетний опыт работы по оснащению лечебных и исследовательских учреждений медицинским оборудованием и расходными материалами самого высокого качества. Мы сотрудничаем как с Государственными, так и коммерческими медицинскими организациями Российской Федерации и стран СНГ. Заказы принимаются оперативно, а доставка товара производится в самые короткие сроки. Наши компетентные сотрудники всегда готовы ответить на все интересующие вас вопросы.
Технические средства реабилитации при нарушении функции выделения
В рамках курса дистанционного образования «Мануальные навыки уролога – советы экспертов» Галина Евгеньевна Тищенко, нейроуролог Реабилитационного центра для инвалидов «Преодоление» и консультант ФГБУ ЦКБ восстановительного лечения ФМБА России, подробно раскрыла тему подбора технических средств реабилитации для людей, страдающих нарушениями выделительных функций.
 | Г.Е. Тищенко нейроуролог Реабилитационного центра для инвалидов «Преодоление» и консультант ФГБУ ЦКБ восстановительного лечения ФМБА России |
Общие сведения о ТСР
Выписка технических средств реабилитации (ТСР) зависит одновременно от двух ведомств: Департаментов здравоохранения и Министерства социальной защиты и труда. Следовательно, некоторые аспекты выписки ТСР связаны с особенностями государственного обеспечения такими средствами граждан с инвалидностью, а также с оформлением медицинской документации.
Технические средства реабилитации – это мероприятия или услуги, которые позволяют инвалиду восстановить или компенсировать утраченные функции организма. Главная цель – позволить пациенту вернуться к бытовой, общественной и профессиональной деятельности в соответствии со структурой его потребностей, кругом интересов, притязаниями, социальным статусом и с учетом реальных возможностей социальной инфраструктуры.
К нарушениям функций выделения относятся нарушения функции выделения мочи – несостоятельность фазы накопления и/или опорожнения мочевого пузыря, а также недержание кала (энкопрез). Как уролог, Галина Евгеньевна подробнее остановилась на первой проблеме.
Большинство лиц с инвалидностью рассматриваемого типа имеет смешанную форму расстройства мочеиспускания, когда страдают как функция наполнения мочевого пузыря, так и функция его опорожнения. В результате у пациента присутствуют и недержание, и хроническая задержка мочи. Таким образом, подбирать средства реабилитации нужно с учетом обоих нарушений:
Перечисленные средства по закону предоставляются гражданам с инвалидностью бесплатно: за счет Министерства социальной защиты или – для москвичей – Департамента здравоохранения города Москвы.
Виды ТСР для опорожнения мочевого пузыря
Прежде чем рассматривать технические средства реабилитации, применяемые при нарушении функции опорожнения мочевого пузыря, нужно упомянуть, что существуют методы компенсации без применения дополнительного оборудования, доступные для пациентов: это рефлекторное мочеиспускание с мануальным пособием: раздражение триггерных зон, приемы Креде и Вальсальвы.
Среди методов с применением ТСР в первую очередь рассматривается постоянное дренирование мочевого пузыря, для чего применяются уретральные и супрапубикальные катетеры. Наконец, может применяться периодическая катетеризация: через мочеиспускательный канал или «сухую стому».
Для постоянной катетеризации, согласно действующему законодательству, применяются следующие виды катетеров:
По этой причине врачу следует точно указывать тип катетера, выписывая его пациенту, чтобы тот в дальнейшем мог получить именно то, что необходимо.
По типу фиксации в мочевом пузыре выделяются:
При выписке ТСР пациенту эти моменты тоже лучше указывать. Пациент в результате должен хорошо понимать, что именно ему нужно, чтобы перечислить все тонкости при заполнении заявки на обеспечение техсредствами. Также необходимо объяснить, что жесткие катетеры не могут назначаться пациенту для самостоятельного использования – такая катетеризация – разовая процедура, выполняемая исключительно врачом в стенах медицинского учреждения.
Периодическая катетеризация выполняется пациентом 4–6 раз в сутки, поэтому крайне важно, чтобы все средства были подобраны правильно, а сама процедура была для человека максимально комфортной.
Согласно классификации ICS (International Continence Society, Международное общество по удержанию мочи), катетеры бывают:
Катетеры из последней группы, по словам Галины Евгеньевны, сегодня признаны наиболее безопасными. Согласно результатам множества международных исследований, они сопряжены с наименьшим риском развития таких осложнений, как микро- и макрогематурия, повреждения слизистой мочеиспускательного канала, развитие сужений и структур уретры. Кроме того, с ними за счет сниженного трения меньше вероятность обострения хронических инфекций нижних мочевых путей, которые в той или иной степени присутствуют у всех пациентов с нарушениями функции мочеиспускания. Наиболее распространенный лубрикант для катетеров такого типа – поливинилпирролидон, абсолютно инертный к человеческому организму и широко применяемый во многих отраслях промышленности. При контакте с водой этот материал становится еще более скользким, следовательно, катетер с покрытием из него – менее травматичным для уротелия.
У пациентов, ведущих активный образ жизни, в законодательной базе прописано к применению еще одно техническое средство – набор-мочеприемник для самокатетеризации. В него входят мешок-мочеприемник, встроенный в него лубрицированный катетер и емкость с физраствором для активации лубриканта. Срок использования такого набора составляет 4 часа, соответственно пациенту необходимо порядка 180 штук на месяц.
Виды ТСР при недержании мочи
Что касается средств, предлагаемых для бесплатного обеспечения при недержании мочи, сегодня из их числа исключены урологические прокладки – их пациентам приходится приобретать на собственные средства. По-прежнему можно получить бесплатно впитывающие пеленки, подгузники и уропрезервативы. О существовании последних, однако, знают далеко не все пациенты, поэтому лечащий врач должен информировать об этом пациентов.
При недержании мочи у мужчин уропрезервативы имеют ряд преимуществ перед подгузниками. В частности, легко надеваются и снимаются без посторонней помощи, в то время как пользователям подгузников часто нужен помощник для надевания и замены. Кроме того, в отличие от подгузников, уропрезервативы не требуют замены в течение 24 часов, защищают кожу от раздражающего действия мочи, не шуршат при движении и незаметны под одеждой, а также не пропускают запах. Таким образом, уропрезервативы способны заметно улучшить качество жизни пациента. Они выпускаются с двумя видами крепления: с пластырем и самоклеящиеся. Кроме того, различаются материалы изготовления: уропрезервативы могут латексными, безлатексными или же с низким содержанием латекса. Здесь требуется индивидуальный подход с учетом индивидуальной переносимости у пациента, а также его личных предпочтений. Иногда мужчине можно рекомендовать использование вместе с уропрезервативами специальных адгезивных салфеток, благодаря которым изделие держится прочнее и меньше травмирует кожу. Также при подборе уропрезерватива необходимо учитывать вероятность спонтанной эрекции. На рынке представлены изделия со свойствами «памяти» и с уплотненными сливными портами, защищающими от перегиба. Помимо этого, необходимо знать, что уропрезервативы имеют размерный ряд и должны подбираться в соответствии с окружностью полового члена пациента. Иногда размеры не соответствуют друг другу у разных производителей, о чем мужчине также нужно помнить, оформляя заявку на получение изделий.
Уропрезервативы крепятся к мешкам-мочеприемникам, которые также выпускаются разного объема: ночные – более вместительные, чем ножные, предназначенные для использования в течение дня и фиксируемые на ноге пациента с помощью ремешков. Эти ремешки также включены в нормативные акты и выдаются бесплатно по две штуки на месяц.
ТСР при недержании кала
Помимо этого, в перечень ТСР, применяемых при нарушении функций выделения входят анальные тампоны, используемые при недержании кала. По сути, они представляют собой механическое препятствие непроизвольному отхождению каловых масс. В неактивном состоянии имеют форму анальной свечи, а при контакте с влагой в прямой кишке их водорастворимая оболочка раскрывается, в результате чего тампон приобретает куполообразную форму. Такие тампоны состоят из вспененного полиуретана, потому легко пропускают газы и не провоцируют вздутие кишечника. Также в них всегда запаян шнур для легкого самостоятельного извлечения. Выпускаются в двух размерах: большом, который предпочтителен при массе тела пациента более 80 кг, и малом – применяемом, в соответствии, у людей весом менее 80 кг. Особо актуальным может быть применение тампонов, когда непроизвольное отделение кала мешает прохождению терапевтических процедур – к примеру, получению гидромассажа.
Некоторые врачи, особенно участковые, семейные, о существовании такого средства не знают и не говорят о нем своим пациентам. Распространение грамотной медицинской информации на этот счет способно существенно повысить качество жизни многих людей и улучшить их социальную адаптацию.
Статья опубликована в журнале «Дайджест урологии» №4 2018, стр. 40-44
Послеоперационное обезболивание. Часть 4. Современные средства обеспечения послеоперационной анальгезии
Основными задачами применения анальгетических средств в послеоперационном периоде являются: устранение страдания, причиняемого болью, создание психологического комфорта и повышение качества жизни пациентов в послеоперационном периоде; ускорение послеоперационной функциональной реабилитации; снижение частоты послеоперационных осложнений; сокращение сроков госпитализации и стоимости лечения.
Нужно отметить, что в настоящее время в большинстве развитых стран неадекватное послеоперационное обезболивание рассматривается как нарушение прав человека и осуществляется в соответствии с принятыми национальными и международными стандартами. В нашей стране во многих клиниках внедрена формулярная система использования лечебных препаратов тех или иных групп, целесообразность применения которых подтверждена данными доказательной медицины, а также обусловлена потребностями и особенностями конкретного лечебного учреждения. Многие авторы полагают, что все хирургические подразделения, а также отделения анестезиологии, реанимации и интенсивной терапии должны иметь в своем арсенале только те анальгетики и анестетики, эффективность и безопасность назначения которых подтверждена доказательствами I (систематизированные обзоры и метаанализы) и II (рандомизированные контролируемые исследования с определенными результатами) уровня (табл. 1).
Таблица 1. Препараты, применение которых для послеоперационного обезболивания обосновано данными доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005).
Группа
Препараты
Дозы, путь введения
Неопиоидные анальгетики, НПВП
Диклофенак
Кетопрофен (Кетонал ®)
Кеторолак (Кеторол ®)
75 мг (150 мг суточная), в/м
50 мг (200 мг), в/м
30 мг (90 мг), в/м
Неопиоидные анальгетики, прочие
1 г (4 г), в/в инфузия в течение 15 минут
Опиоидные анальгетики, сильные
5-10 мг (50 мг), в/в, в/м
20 мг (160 мг), в/в, в/м
Опиоидные анальгетики, слабые
100 мг (400 мг), в/в, в/м
Лидокаин 2%
Бупивакаин (Маркаин®) 0, 25%, 0, 5%
Ропивакаин (Наропин®0, 2%, 0, 75%, 1%
(800 мг суточная) *
(400 мг суточная) *
(670 мг суточная) *
*инфильтрация краев раны, интраплевральное введение, продленная блокада периферических нервов и сплетений, продленная эпидуральная анальгезия.
Мировой опыт послеоперационного обезболивания позволяет выделить следующие основные современные тенденции в борьбе с ПБС:
— широкое применение неопиоидных анальгетиков – нестероидных противовоспалительных препаратов (НПВП) и парацетамола; в различных европейских клиниках частота назначения данных препаратов в качестве базиса послеоперационного обезболивания составляет от 45 до 99%;
— ограничение использования опиоидных анальгетиков, особенно внутримышечного варианта их введения, что обусловлено низкой эффективностью и значительным количеством побочных эффектов данной методики;
— мультимодальный характер послеоперационного обезболивания, т. е. одновременное назначение нескольких препаратов или методов обезболивания, способных воздействовать на различные механизмы формирования болевого синдрома.
Длительность проведения послеоперационного обезболивания является достаточно вариабельной величиной и зависит как от интенсивности болевой афферентации и, следовательно, от травматичности хирургического вмешателсьтва, так и от индивидуальной толерантности пациента к боли. Необходимость целенаправленного купирования ПБС возникает, как правило, в течение первых 4 суток послеоперационного периода (табл. 2).
Таблица 2. Потребность в обезболивании после различных по объему операций.
Хирургическое вмешательство
Продолжительность обезболивания, часы
Вмешательства на верхнем этаже брюшной полости и диафрагме
Вмешательства на нижнем этаже брюшной полости
Операции на тазобедренном суставе
Операции на конечностях
Лапароскопические операции среднего объема
Таблица 3. Методы и средства послеоперационного обезболивания.
1. Традиционное введение опиоидов: внутримышечные инъекции по требованию.
2. Опиоидные препараты агонисты/антагонисты:
а) парентеральное введение опиоидов: внутривенно болюсно, длительная внутривенная инфузия, контролируемая пациентом анальгезия.
б) непарентеральное введение опиоидов: щечное/подъязычное, пероральное, трансдермальное, назальное, ингаляционное, внутрисуставное
3. Неопиоидные анальгетики с системным введением:
а) нестероидные противоспалительные препараты
б) ацетаминофен (парацетамол)
4. Методы регионарной анестезии:
а) эпидуральное введение опиоидов;
б) нестероидные противовоспалительные препараты;
5. Нефармакологические методы:
6. Сочетанное использование представленных методов
Ниже приводятся основные используемые в современной хирургической клинике средства и методы обезболивания с позиций баланса их эффективности и безопасности.
Опиоидные анальгетики.
Данная группа лекарственных препаратов десятилетиями считалась средством выбора для купирования ПБС. Однако в настоящее время опиоидные анальгетики отнюдь не являются «золотым стандартом» в лечени пациентов с острой болью. Тем не менее, по оценкам целого ряда отечественных и зарубежных специалистов, эффективность обезболивания при традиционном назначении опиоидов в качестве монотерапии не превышает 25-30%. Однако постепенное отчуждение от чрезмерной приверженности опиоидам в послеоперационном периоде связана не столько с их недостаточной эффективностью, сколько с целым рядом серьезных побочных эффектов, возникающих при их использовании (табл. 4).
С точки зрения фармакодинамики опиоидные анальгетики являются агонистами или антагонистами различных видов опиоидных рецепторов ЦНС (мю-, дельта-, каппа-). Препараты опиоидной группы активируют эндогенную антиноцицептивную систему (центральная анальгезия), однако не влияют на периферические и сегментарные неопиоидные механизмы ноцицепции и не предотвращают центральную сенситизацию и гиперальгезию. Попытки увеличения эффективности обезболивания и снижения частоты побочных эффектов опиоидных анальгетиков основаны на варьировании способов их введения (в том числе и у одного пациента): внутривенный, внутримышечный, эпидуральный, трансдермальный, сублингвальный, ректальный. Наиболее распространенным, но при этом наиболее небезопасным и наименее эффективным способом введения опиоидов является внутримышечная инъекция. Данная методика наиболее часто приводит к неадекватному обезболиванию – более 60% пациентов отмечают неудовлетворительное качество послеоперационной анальгезии. Причины этого кроются в том, что всем пациентам вводятся фиксированные дозы через стандартные временные интервалы, без учета индивидуальной вариабельности фармакокинетики; часто инъекции опиоидов производятся с большими перерывами, то есть тогда, когда болевой синдром уже выражен и его купирование по определению становится малоэффективным. Именно при внутримышечном введении опиоидов наиболее часто развивается депрессия дыхания, связанная, возможно, с кумуляцией препарата.
Таблица 4. Опиоидные анальгетики при купировании послеоперационного болевого синдрома.
Препарат
Дозировка и пути введения
Относительная анальгетическая активность
Побочные эффекты
Возможны выраженные угнетение дыхания, тошнота, рвота, высокая степень привыкания и максимальный наркогенный потенциал
Угнетение дыхания, тошнота, рвота, высокая степень привыкания и наркогенный потенциал
Угнетение дыхания, тошнота, рвота, наличие привыкания и наркогенного потенциала
Необходимо отметить еще один важный аспект, ограничивающий применение опиоидных анальгетиков в отечественной клинической практике. Использование опиоидных анальгетиков для послеоперационного обезболивания в Российской Федерации строго регламентировано существующими приказами руководящих органов здравоозранения. Например, приказом № 257 Департамента здравоохранения г. Москвы от 2004 г. определяется, в частности, норматив потребления опиоидных препаратов в ампулах на 1 койку различных отделений хирургического профиля в год. Назначение опиоидного препарата как в хирургическом отделении, так и в отделении интенсивной терапии в большинстве ЛПУ сопровождается колоссальным количеством формальных сложностей, что нередко приводит к отказу медперсонала от использования ланных препаратов даже при необходимости назначения опиоидов. По тем же причинам самый современный метод применения опиоидов – контролируемая пациентом аналгезия, в наибольшей степени ориентированная на индивидуальные потребности пациента в обезболивании – в России не получила широкого распространения.
Неопиоидные анальгетики.
Термином «неопиоидные анальгетики» обозначается группа различных по химическому строению, фармакодинамике и, соответственно, механизму обезболивания лекарственных препаратов, применяемых для купирования ПБС с парентеральным, реже пероральным путем введения. Препараты данной группы, используемые как в моноварианте, так и в качестве средства адъювантной терапии, обладают различными анальгетическим потенциалом и совокупностью побочных эффектов (табл. 5).
Таблица 5. Неопиоидные анальгетики для купирования послеоперационной боли.
Класс
Препараты
Особенности терапии
Побочные эффекты
Антагонисты NMDA-рецепторов
Применяется как адъювант при введении опиоидов.
Малые дозы кетамина характеризуются опиоидсберегающим эффектом, повышением качества обезболивания
При использовании в малых дозах – не выражены. Сохраняют побочные эффекты опиоидов.
Антиконвульсанты
Используется как адъювантный препарат в комплексной терапии острой послеоперационной боли. Снижает потребность как в опиоидных, так и внеопиоидных анальгетиках.
Головокружение, сонливость, периферические отеки.
Ингибиторы протеаз
Ингибирование синтеза медиаторов боли на этапе трансдукции, используются как средство адъювантной терапии ПБС
Нерушения в системе гемостаза (гипокоагуляция) – послеоперационные кровотечения.
Центральные α-адреномиметики
Воздействие на трансмиссию и модуляцию боли. Адъювант при опиоидной анальгезии.
Гипотензия, брадикардия, психические нарушения.
Бензодиазепины
Комбинированная терапия с применением феназепама и тизанидина снижает выраженность фантомных болей.
Сонливость, головокружение, психические расстройства
Из приведенных данных становится очевидным, что перечисленные в таблице неопиоидные анальгетики используются лишь как возможное дополнение к базисной терапии опиоидами, использование данных препаратов для купирования ПБС в моноварианте не практикуется.
Формально к группе неопиоидных анальгетиков относятся также нестероидные противовоспалительные препараты (НПВП) и ацетаминофен (парацетамол). Однако вследствие значительной востребованности в современной хирургической клинике данные препараты рассматриваются сейчас как отдельные подклассы средств для купирования ПБС.
Парацетамол.
Несмотря на то, что ацетаминофен (парацетамол) имеет более чем полувековую историю применения в качестве анальгетика и антипиретика, точный механизм действия этого препарата до сих пор не известен. Предполагается наличие центрального механизма действия парацетамола, включающего: подавление активности циклооксигеназы 2 типа в ЦНС, с чем связана профилактика развития вторичной гиперальгезии; подавление активности циклооксигеназы 3 типа, существование которой предполагается и которая, видимо, обладает селективной чувствительностью к парацетамолу; усиление активности нисходящих тормозных серотонинергических путей на этапе модуляции боли.
Потенциально опасным побочным свойством парацетамола является гепатотоксическое и нефротоксическое действие, которое может проявляться при превышении дозы 4 г/сут, особенно при наличии у пациента исходного нарушения функции печени и почек. Ограничениями к применению парацетамола являются: печеночно-клеточная недостаточность с лабораторными проявлениями (повышение уровня трансаминаз), почечная недостаточность, алкоголизм, алиментарная недостаточность, дегидратация.
Местные анестетики.
Важнейшей задачей мультимодальной анальгезии является прерывание афферентного потока ноцицептивных стимулов от периферических болевых рецепторов в органах и тканях к сегментарным структурам ЦНС (задним рогам спинного мозга). Эта задача может быть успешно решена при помощи различных методов регионарной и местной анальгезии. Важную роль в расширении применения методов региональной анальгезии сыграло появление современных местных анестетиков (бупивокаин, ропивокаин), а также детальная отработка методики регионарных блокад.
Эпидуральная анальгезия занимает ключевую позицию среди всех регионарных методов послеоперационного обезболивания. В ходе данной процедуры в эпидуральное пространство на уровне грудного или поясничного отделов позвоночника устанавливается катетер, через который болюсно или путем непрерывной инфузии вводятся местные анестетики. Эпидуральная анестезия является как средством обеспечения анальгезии в ходе операции (в том числе и в моноварианте), так и средством купирования ПБС. Многочисленными исследованиями была доказана принципиально более высокая эффективность продленной послеоперационной эпидуральной анальгезии по сравнению с системным введением опиоидных анальгетиков. Как указывалось выше сами опиоидные анальгетики также могут быть использованы для проведения эпидуральной анестезии. Известно, что эпидуральное введение местных анестетиков и опиоидов достоверно превышает анальгетический эффект использования данных препаратов в отдельности. Тем не менее само по себе эпидуральное введение опиоидов чревато возникновением серьезных побочных эффектов от угнетения дыхания до выраженного кожного зуда. На сегодняшний день принято считать, что преимущества эпидурального введения опиоидных анальгетиков в абдоминальной хирургии не перевешивают риска осложнений самой методики эпидуральной анестезии по сравнению с парентеральным назначением аналогичных препаратов.
Помимо собственно анальгетического эффекта позитивное влияние прослеоперационной продленной эпидуральной анальгезии заключается в прерывании нисходящих симпатических эфферентных импульсов, следствием чего являются улучшение висцерального кровотока (активизация репаративных процессов в зоне вмешательства), повышение активности парасимпатической нервной системы (разрешение пареза пищеварительной трубки).
С точки зрения доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005) преимущества продленной эпидуралной анальгезии включают: более высокое качество обезболивания в сравнении с парентеральным введением опиоидов; улучшение показателей газообмена и снижение частоты послеоперационных легочных осложнений по сравнению с опиоидной анальгезией; ускорение восстановления функции желудочно-кишечного тракта после абдоминальных операций и снижение частоты местных осложнений.
Тем не менее и у эпидуральной анестезии есть ряд существенных ограничений. Сама по себе эпидуральная анестезия является сложной инвазивной процедурой, потенциально опасной в плане развития как местных (инфекционный процесс, повреждение нервных корешков, сосудов паутинной оболочки, твердой мозговой оболочки), так и системных осложнений (депрессия дыхания, кардиотоксические эффекты, артериальная гипотензия). В этой связи проведение эпидуральной анестезии требует наличия специальных навыков у врача-анестезиолога и постоянного мониторинга состояния пациента в отделении интенсивной терапии, реже – в хирургическом отделении.
В последние годы все большую популярность получает методика длительной инфузии местных анестетиков в полость операционной раны. В ходе ряда исследований было показано, что длительная инфузия местных анестетиков в течение 24-48 часов через катетер, установленный в ране, способна повысить качество обезболивания и снизить потребность в опиоидных анальгетиках. Работами отечественных авторов показано, что пролонгированная местная анестезия операционной раны за счет резорбции местного анестетика и присутствия его в плазме в низких концентрациях способна оказывать системный противовоспалительный эффект. Как и в случае эпидуральной анальгезии эффект местных анестетиков при этом обусловлен блокадой не только ноцицептивных путей, но и симпатической иннервации. Говоря о применении пролонгированной местной анестезии операционной раны, следует заметить, что данная методика в настоящее время находится на стадии клинической апробации и ее широкое внедрение изначально ограничивают очевидный риск экзогенного инфицирования раны и реальная опасность системных токсических эффектов местных анестетиков (артериальная гипотензия, аритмии, угнетение дыхания) вследствие их резорбции тканями.
Мультимодальная периоперационная анальгезия.
Из приведенных выше характеристик и, что важнее, недостатков средств и методов купирования ПБС следует очевидное заключение о том, что в настоящее время не существует идеального анальгетика или метода лечения острой послеоперационной боли. Однако приблизиться к решению проблемы адекватности послеоперационного обезболивания вполне возможно, реализуя в клинике концепцию мультимодальной периоперационной анальгезии, предусматривающей одновременное назначение двух и более анальгетиков и/или методов обезболивания, обладающих различными механизмами действия и позволяющих достичь адекватной анальгезии при минимизации побочных эффектов до, во время и после хирургического вмешательства (см. рис. ).
Таблица 6. Варианты схем мультимодальной периоперационной анальгезии, ориентированных на травматичность хирургических вмешательств.